|
|
||||||||||
| Adriana Berenice Silva Gómez y Héctor R. Eliosa León |
|||||||||||
|
Estrés es una palabra de uso común entre la población
humana desde hace décadas. Para la mayoría de la gente es sinónimo de un estado de tensión emocional causado por presiones laborales, económicas, etcétera, que provoca ansiedad, reacciones violentas, enojo y en general un estado de agresividad, entre otras manifestaciones. El estrés no es exclusivo de los seres humanos, también se presenta en animales de vida silvestre y su significado y efecto suele interpretarse de manera diferente. Gracias al incremento del conocimiento sobre el estrés generado por diversas disciplinas científicas es posible integrar lo que aparece disperso en la literatura para conformar lo que se denomina como “ecología del estrés”, cuyos principales aportes provienen de la biomedicina, la ecología, la evolución y la etología. Por tal razón, es necesario uniformar el significado del estrés biológico de manera que incluya su manifestación en todos los animales y que sea de aplicación universal, por lo cual proponemos la siguiente definición: el estrés es un estado fisiológico que se presenta como respuesta a un estímulo amenazante y cuyo objetivo es promover la expresión de conductas o cambios en la fisiología de los órganos y los tejidos corporales que logren la supervivencia del organismo. Ecología del estrés
En la naturaleza existen poblaciones de diferentes especies que interaccionan ecológicamente de diversas maneras; en ocasiones se benefician de manera recíproca, como ocurre en el mutualismo, pero a veces una se beneficia y la otra resulta perjudicada, es el caso de la depredación. A partir de estas interacciones ecológicas se han desarrollado recientemente estudios que aportan información sobre el efecto del estrés en animales silvestres. De acuerdo con algunos investigadores, el estrés se presenta en dos niveles, el individual y el de especie. En el primero, el eje del estrés desempeña un papel clave al permitirle al organismo responder a los cambios y desafíos de su ambiente, considerando tanto los factores bióticos como los abióticos; en el nivel de especie, el eje del estrés es fundamental con relación a las adaptaciones evolutivas ante presiones ecológicas particulares. Al relacionar la información de ambos niveles se obtiene un panorama que permite entender globalmente los efectos del estrés en los vertebrados silvestres.
De acuerdo con diversos autores, la depredación es la mayor fuerza evolutiva que moldea la adaptación de las presas y a la vez resulta ser el mayor estresor biótico para éstas. A pesar de ello, hasta ahora se han desarrollado muy pocas investigaciones que permitan evaluar exclusivamente el efecto del estrés inducido por los depredadores en las presas directamente en la naturaleza, pero sí se dispone de cierta información recabada en el laboratorio. Los resultados obtenidos en ambas condiciones sugieren que el estrés inducido por los depredadores produce diferentes respuestas en las presas en función del tiempo de exposición al factor estresante, la eficiencia del depredador, la fortaleza de la presa, etcétera.
En sentido amplio, se debe considerar que el efecto de la depredación no se reduce a la muerte directa de las presas, sino que también provoca un estrés fisiológico en los sobrevivientes, lo que disminuye la adecuación de las presas. Desde esta perspectiva se ha ido descubriendo, en condiciones controladas de laboratorio, que cuando se colocan liebres hembras preñadas de la especie Lepus americanus en habitaciones de 16 m2 y se introducen jaulas con perros entrenados en su interior, las liebres incrementan su nivel de glucocorticoides fecales (indicador de estrés) y además disminuye significativamente el nacimiento de las crías en comparación con aquéllas hembras que no son expuestas a los perros. Un resultado similar se presenta en hembras de gorriones en las que se simula el efecto de un depredador (robo de huevos del nido). Las hembras sometidas a la remoción frecuente de todos los huevos de su nido depositan un menor número de huevos en la siguiente nidada en comparación con las hembras que no sufren el efecto del depredador. Además de una baja tasa en la puesta de huevos, las hembras que experimentaron depredación frecuentemente evidenciaron mayor desregulación fisiológica. Estos resultados indican que en las presas “el riesgo de la depredación” altera la homeostasis de los organismos, por lo que generan estrategias que les permite superar la presión.
Ante esta situación, puede ser oportuno preguntarse si las experiencias previas de estrés sufrido por las presas en la depredación les provoca una conducta similar a la que desarrollan las personas cuando se exponen a un factor estresante en periodos de tiempo cortos o largos, especialmente si en la última situación se puede reconocer un estrés crónico en los animales silvestres y si se desencadenan los efectos fisiológicos reconocidos en los humanos como enfermedades cardiovasculares, hipertensión, úlceras, ansiedad, miedo, etcétera. Para responder a tales interrogantes se debe tomar en cuenta la siguiente información: los estudios de laboratorio y de campo producen diferentes respuestas de los topos (Myodes gloreolus); en el primer caso, al ser expuestos al olor de las comadrejas (su depredador natural) la presa suprimió su reproducción, en cambio, en el campo no se produce la suspensión de la reproducción, lo que hace pensar que dicha respuesta es un artificio del laboratorio y sugiere que en su ambiente natural los topos no sufren un estrés crónico de los depredadores que impacte de manera crítica su dinámica poblacional.
No obstante, trabajos de campo con la liebre Lepus americanus en Yukón, Canadá, indican que sus poblaciones mantienen ciclos de diez años, en los que se puede apreciar un pico de alta abundancia y otro pico de baja abundancia, este último coincide con un alto riesgo de depredación tanto de aves como de mamíferos. Justo en esta situación se ha sugerido que las liebres están “conscientes” del alto riesgo de depredación que enfrentan, debido a que tienen mayor cortisol libre en el plasma y glucocorticoides fecales, bajos niveles de leucocitos, etcétera; sin embargo, su respuesta al estrés no se vuelve disfuncional ni exhiben síntomas patológicos. En la etapa de mayor riesgo a su supervivencia, las liebres disminuyeron su reproducción, bajando de cuatro a dos crías por hembra como una estrategia para mantener la población, situación que cambia cuando se produce una declinación en las poblaciones de sus depredadores.
Como se puede apreciar, y no obstante la escasa información sobre el tema, los organismos de vida silvestre no manifiestan patologías que repercutan en su salud individual, tal como ocurre en los seres humanos, sino que se ven afectados de manera diferente, principalmente modificando su estrategia reproductiva.
Fisiología del estrés
La condición primordial para el establecimiento del estrés en los individuos es detectar un estímulo dañino (estresor) que altere la homeostasis del individuo; por ejemplo la presencia de un depredador o la escasez de alimento. Una vez que ha sido percibido el estresor, debe alcanzarse la estabilidad interna del organismo mediante el cambio, proceso denominado alostasis y que implica la activación del eje hipotálamopituitarioadrenal (hpa), conocido como el eje del estrés y el consecuente incremento en los niveles de catecolaminas (adrenalina y noradrenalina) y glucocorticoides (cortisol en humanos o corticoesterona en roedores) en sangre y en diferentes tejidos. Las catecolaminas producen el aumento en el tono muscular cardiovascular, el incremento en la frecuencia cardiaca y la rápida movilización de ácidos grasos y carbohidratos, eventos que son de suma utilidad en situaciones en las que el individuo requiere decidir entre “luchar o huir” ante el estímulo estresante. El estrés finaliza cuando el estresor desaparece y los niveles de hormonas retornan a su estado basal.
El sistema del estrés incluye la lenta liberación de cortisol o de corticoesterona de la corteza adrenal y su rápida actividad a través de receptores de membrana en casi todo el organismo. Todo esto se inicia por señales neurales del hipotálamo, el cual secreta la hormona liberadora de corticotropina (crh) lo que, a su vez, promueve la secreción de acth (hormona adrenocorticotrópica) de la glándula pituitaria anterior. Finalmente, la acth induce la síntesis y liberación de cortisol o corticoesterona desde las glándulas adrenales (figura 1).
En general, los glucocorticoides son moléculas promotoras de la gluconeogénesis y se mantienen en altos niveles en la sangre y en diferentes tejidos tales como el cerebral, hasta que el estímulo estresante desaparece. Sin embargo, en condiciones de estrés crónico los glucocorticoides son promotores de la producción de radicales libres y de aminoácidos excitatorios, de la inhibición mitocondrial, de la activación de sistemas de segundos mensajeros y de la disminución de la eficiencia de los mecanismos inmunes y de defensa antioxidante. Estos cambios resultan finalmente en atrofia celular o déficits en la función de los órganos y tejidos afectados, siendo éstas unas de las manifestaciones del estrés crónico.
En momentos sin estrés, el eje hipotálamopituitarioadrenal expresa un mecanismo de retroalimentación negativa, definido como el proceso por el cual el incremento en los niveles de glucocorticoides circulantes activa a los receptores de glucocorticoides del sistema nervioso central para que se inhiba la secreción de la hormona corticotropina. Con esto se reduce la liberación de hormona adrenocorticotrópica de la hipófisis anterior y por tanto también la síntesis y liberación de glucocorticoides desde las glándulas adrenales; con ello la respuesta al estrés se elimina.
Además, el núcleo paraventricular del hipotálamo, el hipocampo y la amígdala ejercen una acción reguladora del eje de manera importante. La glándula pituitaria mantiene la secreción de la hormona adrenocorticotrópica dentro de un rango estrecho de concentración (en picogramos por mililitro) y de manera pulsátil. Las concentraciones de esta hormona en plasma muestran un ritmo circadiano con un pico en la mañana y el punto más bajo de concentración que se presenta alrededor de la media noche. En animales nocturnos, el pico máximo de secreción de la hormona adrenocorticotrópica se expresa al comienzo de la fase de obscuridad. Este ritmo circadiano influye en la liberación de cortisol y corticoesterona. Ambos glucocorticoides, alcanzan un pico de concentración al despertar y los niveles más bajos antes o durante el sueño. Estas hormonas en su estado libre o unidas a transcortina ejercen una acción inhibitoria el cerebro y sobre las glándulas adrenales con lo que se logra la disminución en la liberación de la hormona adrenocorticotrópica.
El papel de estrés en la evolución
En los ejemplos antes señalados, de las liebres y los topos, se puede apreciar que en los casos en que no se produce la muerte directa de las presas por parte del depredador, la respuesta al estrés inducida exclusivamente por el riesgo de depredación varía en algunas presas, como en las liebres que disminuye su adecuación, pero en otras, como en los topos, la reproducción no se ve afectada, por lo que se puede señalar que existe una plasticidad de respuestas al estrés crónico de largo tiempo. Por otra parte, se debe tomar en cuenta que en las presas de vida silvestre el riesgo de depredación no provoca una patología fisiológica severa y que mucho menos se fija en el linaje a lo largo del tiempo, ya que de ser así, dicha patología sería eliminada por la selección natural.
En los casos más extremos de riesgo de depredación para las presas se ha desarrollado una disminución en la adecuación de las presas (reproducción y supervivencia) como una adaptación para asegurar que la población se mantenga en el tiempo. Por tal razón, el eje de respuesta fisiológica del estrés se fija de manera diferenciada en las presas, además existen otros factores que pueden incrementar o disminuir la intensidad del estrés, como la baja disponibilidad de alimento o de sitios de reproducción, así como condiciones abióticas severas que también influyen en la respuesta de las presas.
Adicionalmente, se debe considerar que los estilos de defensa de las especies varían de una a otra, y que esto ocurre incluso al interior de la misma especie. No obstante, esta situación parece indicar que el eje hipotálamopituitarioadrenal es un sistema de respuesta conservada evolutivamente en los vertebrados que ajusta de manera fina el funcionamiento de las especies de acuerdo con las condiciones ambientales que prevalecen en el tiempo.
|
|||||||||||
|
Referencias Bibliográficas
Abidin, Ismail et al. 2004. “The effect of chronic restraint stress on spatial learning and memory: relation to oxidant stress”, en International Journal Neuroscience, vol. 114, núm. 5, pp. 683-699.
Boonstra, Rudy. 2013. “The ecology of stress: a marriage of disciplines”, en Functional Ecology, vol. 27, núm. 1, pp. 711. Clinchy, Michael, Michael J. Sheriff y Liana Y. Zanette. 2013. “Predatorinduced stress and the ecology of fear”, en Functional Ecology, núm. 27, pp. 56-65. Nesse, R. M., S. Bhatnagar y E. A. Young. 2010. “Evolutionary origins and functions of the stress response”, en Encyclopedia of Stress, George Fink (ed.). Academic Press Ed., San Diego. Pp. 965-970. |
|||||||||||
| _____________________________ |
|||||||||||
| Adriana Berenice Silva Gómez Escuela de Biología, Benemérita Universidad Autónoma de Puebla. Es bióloga por la Benemérita Universidad Autónoma de Puebla. Realizó sus estudios de maestría en ciencias fisiológicas en el Instituto de Fisiología de la BUAP e hizo el doctorado en Investigación en Medicina en la Escuela Superior de Medicina del Instituto Politécnico Nacional. Desde 1999 es profesora en la Escuela de Biología de la buap. Su interés académico radica en la fisiología del sistema límbico y conducta en ratas. Héctor R. Eliosa León Escuela de Biología, Benemérita Universidad Autónoma de Puebla. Estudió la licenciatura en biología y es maestro en ciencias por la Facultad de Ciencias de la UNAM. Desde 1991 es Profesor-Investigador de la Escuela de Biología de la Benemérita Universidad Autónoma de Puebla. Imparte los cursos de Biología animal II, Zoología de vertebrados, Sistemática y Biogeografía. |
|||||||||||
| _____________________________ | |||||||||||
|
cómo citar este artículo →
Silva Gómez, Adriana Berenice y Héctor R. Eliosa León. 2016. El estrés en vertebrados silvestres, su efecto fisiológico y evolutivo. Ciencias, núm. 120-121, abril-septiembre, pp. 22-28. [En línea]. |
|||||||||||
| de la solapa |
|
|||||||||||||
|
¿Darwin para niños?
|
 |
|||||||||||||
|
Darwin and Evolution for kids. His life and Ideas. With 21 activities.
Kristan Lawson.
Chicago Rewiew Press.
Baltimore, 2003. |
||||||||||||||
|
Podemos considerar que el libro que ahora comento
forma parte de lo que Maura C. Flannery llamó, en tono algo peyorativo, la “Industria Darwin” o la “Factoría Darwin”, haciendo referencia a la enorme y creciente cantidad de publicaciones existentes sobre la vida, obra y milagros (me atrevería a decir) de Charles Darwin. Ahora bien, entre los dieciocho títulos que Flannery cita en su artículo ninguno está específicamente dirigido al lector más joven. Así pues, la obra de Lawson, objeto de mi reseña, podría contribuir a llenar este vacío en la literatura sobre el pensamiento evolucionista. Darwin and Evolution for Kids es un libro profusamente ilustrado con láminas y fotografías tanto antiguas como actuales. Arranca con una nota de advertencia para los lectores ávidos por conocer más sobre evolución y que no quieran perder su tiempo leyendo sobre la historia vital de Darwin: de ser así, pueden encontrar una sencilla explicación de la teoría de Darwin en el sexto capítulo. Antes de seguir, me apresuro a señalar que, como lo aclaró Ernst Mayr en su libro What Evolution Is, “la teoría de Darwin” no existe en cuanto a una única teoría científica.
En realidad, las ideas de Darwin sobre la evolución se estructuran en torno a un conjunto de diferentes teorías interrelacionadas, que pueden entenderse mejor si se las explica de modo separado. Éstas son: 1) el cambio de los seres vivos a lo largo del tiempo, lo que usualmente se denomina evolución y que técnicamente se corresponde con la evolución anagenética, que no produce aumento en el número de especies dentro de un linaje determinado; 2) la descendencia de todos los seres vivos de un ancestro común remoto, que se manifiesta en el conocido patrón con forma de árbol, de arbusto o de coral que se ramifica; 3) la gradualidad con la que tiene lugar el cambio evolutivo a lo largo del tiempo, es decir, la ausencia de discontinuidades y saltos en el proceso evolutivo; 4) la multiplicación de especies, o sea, el origen de la diversidad biológica o especiación, y que se corresponde con la evolución cladogenética, que sí produce aumento en el número de especies de un linaje; y 5) la selección natural, el principal “motor” de la evolución y el único conocido capaz de generar las maravillosas adaptaciones de los seres vivos a su medio ambiente biótico y abiótico.
Asimismo en el libro se muestra una línea de tiempo que permite situar cronológicamente varios pasajes importantes en el desarrollo histórico del pensamiento evolutivo. Desde el año 1654, cuando el arzobispo James Ussher, siguiendo las genealogías del Antiguo Testamento, se atrevió a calcular la antigüedad del mundo y concluyó que el acto sobrenatural de creación por dios tuvo lugar, ni más ni menos, el anochecer previo al domingo 23 de octubre del año 4004 a. C.; hasta llegar a 1953, cuando se publicó el artículo de James D. Watson y Francis Crick en la prestigiosa revista científica Nature, que describió por vez primera la estructura doble helicoidal de la molécula de adn.
Los primeros cinco capítulos son de lectura amena, sobre la vida y la obra de Darwin; en el 6 se explica “la idea que cambió el mundo”. En 7 y 8 se expone lo que le ocurrió a Darwin y al mundo tras la publicación de El origen de las especies en 1859.
El libro cierra con un bloque final que incluye un glosario con el significado de algunos términos técnicos (como los conceptos de adaptación o selección sexual), más una colección de recursos didácticos, siete direcciones en la red, una lista de referencias bibliográficas y un índice.
Además, intercaladas aquí y allá en el texto hay instrucciones para realizar ventiún actividades sencillas —y divertidas, según la contraportada del libro— que los jóvenes lectores pueden completar para comprender mejor algunos puntos del texto. Éstas van desde elaborar una especie de análisis taxonómico de diferentes seres hasta un juego que se basa en el “Juicio del Mono”, el famoso Monkey Trial de 1925 en el que se juzgó al profesor de instituto John Scopes por haber enseñado la teoría de la evolución de Darwin en sus clases de ciencia, en contra de las leyes de la época en el estado de Tennessee.
El libro incluye también varias actividades propias de un geólogo o de un naturalista de campo, como Darwin; se simula la formación de los fósiles (usando arcilla o plastilina y moldes sencillos), la deposición de estratos geológicos (con harina, café y azúcar, entre otros ingredientes); las actividades llevan a estudiar cómo las plantas carnívoras atrapan a sus presas con “atrapamoscas” y las consumen, como las de la familia Droseraceae, entre otros ejemplos.
Encuentro que el libro es difícilmente legible por los niños de nueve años a los que se supone que va dirigido. De hecho, los temas tratados y la profundidad con la que se exponen me recuerdan a otros libros sobre la vida y la obra de Darwin que he leído recientemente como Darwin y la evolución de Paul Strathern o Charles Darwin: the Concise Story of an Extraordinary Man de Tim Berra, que no están destinados al público más joven. En favor a la verdad, sólo las actividades del libro de Lawson están dirigidas específicamente a los niños. Así pues, aunque creo que el libro no cumple su objetivo de acercar la figura y la obra de Darwin a los niños, sí puede ser leído sin problema por un lector adulto interesado en el tema, incluso sin haber tenido ningún contacto previo con la figura de este gran pensador: quizás el más importante en la historia de la ciencia, con el permiso de Newton.
|
||||||||||||||
|
Referencias bibliográficas
Berra, Tim M. 2008. Charles Darwin. The Concise Story of an Extraordinary Man. The Johns Hopkins University Press, Baltimore. Flannery, Maura C. 2006. “The Darwin Industry”, en The American Biology Teacher, vol. 68, núm. 3, pp. 163-166. Mayr, Ernst. 2000. “Darwin’s influence on modern thought”, en Scientific American, núm. julio, pp. 78-83. _____. 2001. What Evolution Is. Phoenix, Londres. Strathern, Paul. 2001. Darwin y la evolución. Siglo XXI, Madrid. |
||||||||||||||
| _______________________________________________ | ||||||||||||||
| José Antonio González Oreja Departamento de Ciencias Biológicas, Universidad Popular Autónoma del Estado de Puebla. |
||||||||||||||
| _________________________________________________ | ||||||||||||||
|
cómo citar este artículo →
González Oreja, José Antonio. 2016. ¿Darwin para niños? Ciencias, núm. 120-121, abril-septiembre, pp. 154-155. [En línea].
|
||||||||||||||
 |
|
||||||||||
| Manuel Feria Ortiz |
|||||||||||
|
Desde hace varias décadas se ha observado un interés
creciente por realizar estudios filogenéticos moleculares. En un principio se utilizaron con mayor frecuencia datos de secuencias de proteínas o de sitios de restricción, pero desde la implementación de los métodos de secuenciación de adn a finales de los setentas y en particular desde que se comenzó a utilizar la reacción en cadena de la polimerasa ha habido un aumento en el uso de datos de secuencias de ácidos nucleicos (nucleares o de organelos celulares). Actualmente, los datos de secuencias representan una herramienta rutinaria dentro de muchos campos de la biología y su uso en la inferencia filogenética ha tenido un impacto considerable en la sistemática de una gran diversidad de organismos. La preponderancia en el uso de secuencias de adn (o arn) en estudios filogenéticos se debe a varios factores; uno de ellos consiste en el gran poder resolutivo de los datos de secuencias. Los genomas nucleares y extranucleares (de mitocondrias y cloroplastos) ofrecen una enorme gama de caracteres. Además, diferentes segmentos del genoma pueden poseer propiedades diferentes y ser útiles en la resolución de problemas distintos; por ejemplo, mientras que algunas secuencias permiten investigar relaciones filogenéticas a nivel poblacional o de especies cercanamente emparentadas (como adn de mitocondrias), otras permiten valorar las relaciones de grupos tan distantes como filos o reinos (genes nucleares que codifican para ribosomas). Otro factor importante para el predominio en el uso de secuencias de adn consiste en la gran variedad de métodos que se han propuesto para inferir y evaluar árboles filogenéticos a partir de datos de estas secuencias. También es necesario señalar el desarrollo en la tecnología de cómputo, pues paralelamente a la obtención y acumulación de datos de secuencias ha mejorado enormemente la capacidad de procesamiento de los equipos de cómputo y se ha implementado una variedad de programas que permiten obtener árboles a partir de los métodos de inferencia propuestos.
Elección de secuencias
La aplicación de algún método de inferencia, por efectivo que sea, no garantiza por sí mismo la obtención de resultados confiables. La eficiencia de cualquiera de los métodos disponibles depende no sólo de sus propias cualidades sino también de la calidad, elección y obtención de los datos. Si los datos no son adecuados para el problema que se estudia, entonces los resultados serán espurios. En el caso de datos de secuencias la elección consiste en cuál segmento de adn o arn ha de utilizarse, el de un gen o el de una secuencia particular, por lo que es uno de los aspectos más importantes en cualquier estudio filogenético molecular.
Uno de los aspectos más importantes a considerar cuando se elige un gen es su tasa de evolución, que ésta sea adecuada o que no dependa del grupo particular bajo análisis. Si la tasa de evolución de un gen es relativamente alta y los tiempos de divergencia de los taxones involucrados son muy extensos (como en el caso de taxones lejanamente emparentados) se espera que la variación dentro de un sitio nucleotídico particular no refleje adecuadamente el cambio evolutivo ocurrido en el mismo. Esto es así debido a que si la tasa de sustitución es alta y el tiempo transcurrido es relativamente largo hay oportunidad para que en un mismo sitio (de un mismo gen) hayan ocurrido varias sustituciones. Este hecho puede conducir a inferencias erróneas; por ejemplo, si dos secuencias tuvieran el nucleótido citosina en una determinada posición podría asumirse erróneamente que no ha habido cambio evolutivo en dicho sitio cuando realmente han ocurrido varias sustituciones, pero éstas han ocurrido de tal manera que ahora las dos secuencias poseen el mismo nucleótido, (esto es, que han convergido hacia el mismo nucleótido).
Alineación
Otro paso crítico en un análisis filogenético consiste en manejar los datos disponibles de tal modo que se obtenga una matriz de datos confiable y que pueda ser leída por los paquetes de cómputo disponibles. El que sea confiable implica que los caracteres involucrados sean legítimamente comparables, lo que en sistemática implica que sean potencialmente homólogos. En el caso de caracteres morfológicos el manejo de los datos incluye principalmente la delimitación, codificación y ordenación de los estados de carácter, así como la ponderación de caracteres y estados de caracteres. En el caso de datos de secuencias, los caracteres que se van a utilizar consisten en los sitios nucleotídicos presentes a lo largo de la misma (o los sitios correspondientes a los aminoácidos en el caso de proteínas), y los nucleótidos o aminoácidos presentes en cada sitio particular. En consecuencia, en el caso de datos de secuencias, el manejo preliminar de los datos consiste en obtener una matriz en la cual las filas sean las secuencias correspondientes a los taxones bajo análisis y las columnas los caracteres (sitios nucleotídicos) involucrados en el análisis. Esto implica acomodar las secuencias de tal modo que todos los nucleótidos que queden en una columna particular sean homólogos entre sí. A este proceso se le denomina alineación e involucra varias hipótesis de homología, una por cada posición de nucleótido.
La alineación de una serie de secuencias no es un problema trivial. Si bien en algunos casos puede ser sencillo en otros llega a convertirse en un problema analítico del mismo orden de complejidad que la inferencia filogenética. Por esta razón, como ha ocurrido en el caso de los métodos de inferencia filogenética, se ha propuesto una variedad de métodos de alineación de secuencias que poseen diferentes ventajas y desventajas; asimismo, debido a que en muchos casos el proceso de alineamiento se realiza antes de la aplicación de un método de inferencia, las relaciones filogenéticas que finalmente se obtengan dependerá en gran medida del método de alineación que se utilice. De hecho, muchos autores consideran que la filogenia resultante depende más del método de alineamiento que del método de inferencia que se utilice.
La necesidad de alinear las secuencias de nucleótidos se debe a la ocurrencia de mutaciones puntuales (sustituciones) y de eventos de inserción o deleción llamados “indeles” (contracción de estas palabras). Si no hubiera indeles, la longitud de un gen o segmento de nucleótido particular (o de aminoácidos en el caso de proteínas) sería la misma en todos los organismos que lo tuvieran. En consecuencia, todas las secuencias tendrían las mismas posiciones y todos los nucleótidos presentes en una posición o columna particular serían homólogos entre sí; en tal caso, evidentemente cada posición representaría un carácter para el análisis filogenético y no habría motivo para intentar realizar una alineación. Por otro lado, si sólo ocurrieran eventos de inserción o deleción el alineamiento de las secuencias sería un proceso muy sencillo, únicamente tendrían que acomodarse las secuencias de tal modo que en cada posición se encontraran siempre los mismos nucleótidos, una situación en la que la única fuente de información filogenética serían los indeles (huecos en las alineaciones) y la reconstrucción filogenética, si fuera posible, requeriría secuencias extremadamente largas con el fin de que se incluyera una cantidad suficiente de indeles filogenéticamente informativos.
La ocurrencia de diferentes tipos de mutaciones provoca que se obtengan secuencias de distinta longitud, que los nucleótidos homólogos no sean los mismos en cada secuencia considerada y que éstos se encuentren desfasados con respecto de la posición homóloga a la cual pertenecen. En consecuencia, la alineación consiste básicamente en detectar en qué posiciones debieron haber ocurrido eventos de inserción o deleción y ubicar espacios en dichos sitios a fin de que cada posición incluya únicamente nucleótidos homólogos. Realmente no es posible asegurar la homología de los nucleótidos presentes en un sitio determinado; esto implicaría asegurar que los nucleótidos presentes en el sitio derivan de un mismo nucleótido presente en una secuencia antecesora, lo cual es imposible de saber. La alineación, por lo tanto, consiste en el establecimiento de hipótesis de homología de estados de carácter (una para cada posición de la secuencia), y es un paso fundamental en el análisis filogenético de las secuencias de nucleótidos. Como se señaló antes, los errores en esta fase del análisis se verán reflejados en todos los análisis subsecuentes (obtención de árboles, valoración de los mismos, etcétera), al margen del rigor con el que se realicen.
En la práctica, el alineamiento de secuencias correspondientes a taxones cercanamente emparentados o de secuencias de genes que codifican proteínas es normalmente sencillo; estas secuencias son comúnmente muy similares entre sí en virtud del poco tiempo transcurrido desde su divergencia. La similitud en las secuencias facilita su alineación. En el caso de secuencias de genes que codifican proteínas, las inserciones o deleciones son raras y generalmente afectan a tres —o a algún múltiplo de tres— sitios nucleotídicos (de otro modo se alteraría drásticamente el marco de lectura del gen bajo alineación). Por lo tanto, a menos que la divergencia entre las secuencias sea muy alta, la alineación de genes que codifican proteínas generalmente no presenta problemas.
Contrariamente, los segmentos de adn no codificadores, tales como los intrones o aquellos segmentos que se encuentran entre genes, son particularmente problemáticos de alinear. En tales casos, sobre todo en secuencias muy divergentes, es típicamente común la ocurrencia de los tres tipos de mutaciones: insersiones, deleciones y sustituciones. En consecuencia, las secuencias involucradas comúnmente poseen longitudes muy diferentes y existen muy pocos sitios conservados, esto es, muy pocos sitios en donde todas las secuencias poseen el mismo nucleótido; esto impide enormemente el alineamiento debido en particular a la dificultad de determinar los sitios exactos en los que ocurrieron los indeles.
Métodos de alineación de secuencias
Algunos autores han alineado las secuencias “a mano”. Es frecuente que el investigador se base en el conocimiento de la estructura de la molécula codificada por la secuencia en cuestión para alinear sus secuencias. En el caso de secuencias que codifican proteínas, la alineación debe mantener el marco de lectura que produce la proteína en cuestión; por lo tanto, una manera de verificar la alineación consiste en convertir las secuencias de nucleótidos en secuencias de aminoácidos y corregir las inconsistencias, es decir, los cambios en el marco de lectura por la introducción de huecos únicos. Sin embargo, la alineación manual sólo es posible en el caso de que haya relativamente pocos indeles y las secuencias no sean muy divergentes. Comúnmente, aun en el caso de secuencias de genes que codifican para proteínas, la ocurrencia de sustituciones y algunos indeles complica el proceso, de modo que se vuelve impráctica la alineación manual. Por esta razón, en prácticamente todos los casos la alternativa más viable es la utilización de algún algoritmo matemático. Aun así, con el fin de obtener una matriz de datos más confiable, es frecuente que un investigador utilice algún algoritmo y posteriormente afine las secuencias obtenidas “a mano”. Con frecuencia tales ajustes también se realizan con base en el conocimiento de la estructura secundaria de la molécula producida por las secuencias en cuestión.
Se han propuesto diversos algoritmos para alinear secuencias de nucleótidos y muchos de éstos están diseñados para comparar y alinear parejas de secuencias. Sin embargo, si el propósito es realizar estimaciones filogenéticas, necesariamente se tienen que alinear más de dos secuencias. La mayoría de los algoritmos diseñados para alinear secuencias múltiples se basa en el algoritmo de alineación descrito en 1970 por Needleman y Wunsch, en el cual se asignan valores positivos a las coincidencias positivas (el mismo nucleótido en ambas secuencias), y cero o valores negativos a las coincidencias negativas (los nucleótidos involucrados son diferentes). Debido a la facilidad con la que pueden insertarse huecos de tal modo que se obtengan solamente coincidencias positivas, se hace necesario penalizar la introducción de los mismos en el proceso de alineamiento. En consecuencia, a los huecos se les asigna comúnmente un valor negativo mayor que el asignado a las coincidencias positivas; no obstante, los huecos de más de una posición no se penalizan normalmente en proporción directa a su tamaño. La razón es que es más probable que dos o más nucleótidos se inserten o eliminen simultáneamente a que ocurran dos o más indeles independientes en sitios contiguos.
El procedimiento usual en muchos algoritmos de alineación múltiple consiste en alinear progresivamente las secuencias: primero se alinea un par de secuencias y después se van agregando y alineando una a una las demás hasta obtener todas las secuencias alineadas. Sin embargo, dado que la alineación final depende del orden en el que se agreguen las secuencias, una estrategia consiste en realizar alineaciones para pares de secuencias y, con base en sus similitudes, obtener un árbol que sirva de guía para decidir el orden con el que se alinearán las secuencias.
Otra estrategia consiste en realizar simultáneamente la alineación y el análisis filogenético, y una más se basa en la idea de que el alineamiento y la inferencia filogenética tienen una meta común y por lo tanto no deben de ser procedimientos independientes. La implicación es que el alineamiento y la inferencia filogenética deben ser procedimientos ligados y el primero no debe preceder al segundo.
Actualmente existen muchos programas de cómputo que permiten realizar alineamientos de datos de secuencias (de nucleótidos o aminoácidos), los cuales ejecutan algún algoritmo como los señalados previamente y una matriz de secuencias alineada. Ciertos programas, como ClustalX o W, pueden bajarse gratuitamente de la red. Otros, sin embargo, tales como mega, tiene un costo y deben pagarse antes de poder ser utilizados plenamente.
Alineaciones problemáticas
En muchos casos es difícil estar seguro de que se ha obtenido una alineación confiable, particularmente cuando la divergencia entre las secuencias es grande y su alineación requiere la incorporación de muchos huecos. La razón es que cuando ha habido mucha divergencia entre las secuencias, diferentes combinaciones de parámetros (costos de sustitución y penaltis de huecos y extensión de huecos) pueden dar alineamientos distintos y es difícil precisar cuál de todos ellos es el más confiable. Ante esta situación es necesario verificar la alineación y en su caso modificarla con el fin de obtener una alineación razonable. Como ya se señaló, dicha verificación puede realizarse “a ojo” o con base en la estructura secundaria de la molécula codificada. No obstante, deben justificarse claramente todas las modificaciones que se realicen.
Por otro lado, una situación común en muchos estudios filogenéticos es que las secuencias contengan regiones en las cuales no sea posible identificar adecuadamente las columnas de nucleótidos homólogos. La mayor parte de los investigadores simplemente borran estas regiones debido a que sus caracteres o posiciones pueden ser engañosos o contener muy poca información filogenética. No obstante, aun las regiones más problemáticas pueden contener información filogenéticamente útil y resulta difícil delimitar objetivamente qué secciones son ambiguas y cuáles confiables.
Se han propuesto diferentes procedimientos para tomar en cuenta las regiones ambiguas. Uno consiste simplemente en producir todos los alineamientos posibles para un intervalo de parámetros de alineamiento particular y, posteriormente, se obtiene un árbol para cada alineamiento y se aceptan únicamente los clados que estén presentes en todos los árboles. Otro método es el de elisión, que consiste en obtener dos o más alineamientos y concatenarlos en una matriz única más grande. De este modo, automáticamente se le da más peso a las posiciones no ambiguas (que resultan similares en todas las alineaciones) y menos a las más ambiguas que podrían aparecer, por ejemplo, en sólo una de las alineaciones.
En otro método, denominado fixed caracter state o fragmentlevel alignment, las regiones ambiguamente alineadas se tratan como caracteres multiestado; los estados de cada carácter consisten en las variantes de secuencia distintas encontradas. Posteriormente se construye una matriz de pasos para asignarle un costo a la trasformación de un estado en otro (esto es, el cambio de una variante de secuencia en otra) y dicho costo se calcula con base en las sustituciones y huecos que se requieren para transformar un estado en otro. De este modo, las transformaciones entre estados muy divergentes tienen costos más altos.
Si bien todos estos métodos presentan ventajas y desventajas representan una alternativa viable a la simple eliminación de las regiones problemáticas.
|
|||||||||||
|
Referencias Bibliográficas
Doyle, Jeff J. y Jerrold I. Davis. 1998. “Homology in molecular phylogenetics: a parsimony perspective”, en Molecular Systematics of Plantas II. dna sequencing, Soltis, Douglas, Pamela Sotis y Jeff J. Doyle (eds.). Kluwer Academic Publishers, Londres. Pp. 101-131.
Felsenstein, Joseph. 2004. Inferring phylogenies. Macmillan Education, Massachusetts. Lemey, Philippe, Marco Salemi y Anne-Mieke Vandamme. 2009. The phylogenetic handbook. A practical approach to phylogenetic. Analysis and hypothesis testing. Cambridge University Press, Cambridge. Lutzoni, François et al. 2000. “Integrating ambiguously aligned regions of dna sequences in phylogenetic analysis without violating positional homology”, en Syst. Biol., vol. 49, núm. 4, pp. 628–651. Morrison, D. A. y J. T. Ellis. 1997. “Effects of nucleotide sequence alignment on phylogeny estimation: a case study of 18S rdnas of Apicomplexa”, en Molecular Biology Evolution, vol. 14, núm. 4, pp. 428–441. Nei, Masatoshi y Sudhir Kumar. 2000. Molecular evolution and phylogenetics. Oxford University Press, Nueva York. Rosenberg, S. M. 2009. “Sequence alignment. Concepts and history”, en Sequence alignment. Methods, models, concepts, and strategies, Rosenberg, Michael S. (ed.). University of California Press, Londres. Pp. 1–22. Scotland, Robert y R. Toby Pennington (eds.). 2000. Homology and systematics. Taylor and Francis, Londres. Swofford, David L. et al. 1996. “Phylogenetic inference”, en Molecular Systematic, Hillis, David M., Craig Moritz y Barbara K. Mable (eds.). Sinauer Asociates, Sunderland. Pp. 407–514 Wheeler, Ward C. 1995. “Sequence alignment, parameter sensivity, and phylogenetic analysis of molecular data”, en Systematic Biology, vol. 44, núm. 3, pp. 321–331. |
|||||||||||
| _____________________________ |
|||||||||||
| Manuel Feria Ortiz Museo de Zoología, Facultad de Estudios Superiores-Zaragoza, Universidad Nacional Autónoma de México. Se recibió como biólogo en la Facultad de Estudios Superiores Zaragoza, UNAM en 1986. Realizó sus estudios de maestría y doctorado en la Facultad de Ciencias, también en la UNAM. Actualmente es Profesor de Carrera Titular “A” de tiempo completo y desde 1990 es responsable de la colección de anfibios y reptiles de la FES-Zaragoza. A partir de su ingreso a la Facultad ha impartido las materias de evolución y taxonomía que forman parte del plan de estudios de la carrera de Biología. Como investigador se ha dedicado principalmente al estudio de anfibios y reptiles. |
|||||||||||
| _____________________________ | |||||||||||
|
cómo citar este artículo →
Feria Ortiz, Manuel. 2016. Alineación e interferencia filogenética. Ciencias, núm. 120-121, abril-septiembre, pp. 142-149. [En línea].
|
|||||||||||
| de la vida |
|
|||||||||||||
|
Almacenamiento
de esperma: ¡las hembras lo hacen! |
 |
|||||||||||||
|
Claudia Olivera, José Jaime Zuñiga, Marcela Villagrán
y Norma A. Moreno M. |
||||||||||||||
|
¿Creerías que las hembras de algunos animales
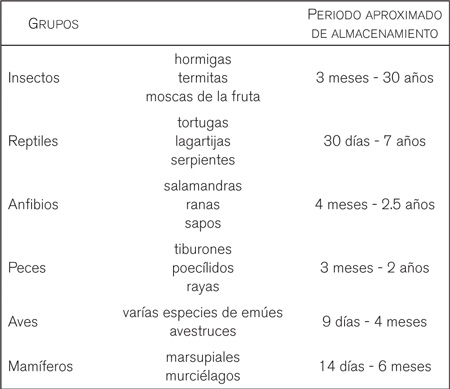
pueden guardar el esperma de los machos por largos periodos de tiempo? Si tu respuesta es no, estás equivocado; de hecho, muchísimos años de evolución han provocado este fenómeno reproductivo llamado retención de esperma, el cual consiste en la capacidad de las hembras para almacenar espermatozoides saludables en alguna parte del tejido de su aparato reproductor. Dicha retención se presenta en varios grupos de insectos, anfibios, reptiles, peces y algunos mamíferos (cuadro 1). El tiempo de retención de esperma puede variar entre sólo algunas horas hasta años después de que la hembra se aparea con un macho; por ejemplo, las abejas y termitas reinas pueden guardar el esperma durante casi toda su vida (décadas). Por el contrario, la mayoría de las hembras de mamíferos retienen el esperma del macho sólo un par de horas, como es el caso de los cerdos y las ovejas.
Los animales que retienen esperma por más tiempo son los insectos; particularmente las hormigas reina conocidas por su longevidad, de aproximadamente treinta años, que se aparean cuando son adultas jóvenes y retienen millones de espermatozoides vivos dentro de su aparato reproductor, incluso después de morir; de hecho, nunca más vuelven a aparearse y cuando las hormigas reinas establecen una colonia, viven décadas fertilizando sus huevos con los espermatozoides almacenados. Los machos mueren en el día que se aparean con la reina, dejando su valiosa carga genética para que pase de generación en generación durante toda la vida reproductiva de la hembra. Otro ejemplo de insectos que puede retener esperma, y de los más estudiados en el mundo científico, son esas mosquitas que están alrededor de los plátanos: Drosophila melanogaster.
Algunos anfibios como las salamandras pueden retener esperma por largo tiempo; por ejemplo, el increíble tritón (Triturus vulgaris) es capaz de retener el esperma durante tres o cuatro meses. De manera similar, la salamandra (Notophthalmus viridescens) llega a almacenar esperma un poco más de tiempo, aproximadamente durante seis meses.
El grupo de los reptiles no se queda atrás, pues tiene el segundo lugar en almacenar esperma más tiempo. Existen alrededor de veintisiete especies de serpientes que retienen esperma por varios años. Otro caso es la serpiente acuática Acrochordus javanicus, cuyo esperma puede ser retenido en las hembras durante siete años. Por su parte, las tortugas sólo lo retienen por un tiempo aproximado de cuatro años, y en lagartijas hay once especies distintas que pueden retener esperma desde algunos días hasta varios meses.
En el mar existen once especies de tiburones cuyas hembras pueden almacenar espermatozoides durante años. Otros organismos más pequeños pueden retener esperma varios meses, como los peces vivíparos (no ponen huevos, sino que producen crías completamente desarrolladas) que se encuentran en los ríos, como los guppies, mollies, platies y peces cola de espada.
En las alturas existen treinta y dos especies de aves que retienen esperma desde días hasta meses, como algunas aves marinas solitarias que pueden retenerlo sesenta días.
Finalmente, en mamíferos existen alrededor de once especies de murciélagos, como Myotis lucifugus, en las que el esperma es retenido por seis meses, y un caso cercano son nuestras mascotas, pues las hembras de los perros llegan a almacenar esperma durante once días.
¿Dónde se almacena?
Los lugares en donde se retiene el esperma dentro de las hembras y las formas en las que se almacena varían entre las distintas especies y resultan en diferentes estructuras especializadas dentro de la hembra. En salamandras, por ejemplo, la retención de esperma ocurre en glándulas tubulares de la cloaca llamadas espermatecas; debido a la forma y a las sustancias que secretan, son estructuras especializadas en retener el esperma en buenas condiciones por mucho tiempo. Pequeños peces como los guppies, mollies y charales también retienen esperma en sus espermatecas que, a diferencia de las salamandras, se localizan dentro del ovario de la hembra; allí las cabezas de los espermatozoides tienen una estrecha relación con el tejido ovárico y sus colas se orientan hacia el centro de la espermateca.
Las hembras de la mosca de la fruta Drosophila melanogaster retienen esperma por medio de células especializadas llamadas secretoras de espermatecas, cuya principal función es mantener el esperma saludable dentro de la hembra. Por otro lado, en las ranas y los sapos el esperma es almacenado en el oviducto, conducto que comunica el ovario con el exterior del cuerpo del animal; justo ahí, existen estructuras especializadas llamadas túbulos de almacenamiento de esperma. De igual manera, las hembras de reptiles como tortugas, lagartijas y serpientes retienen el esperma en túbulos de almacenamiento que se encuentran en diferentes partes del oviducto.
En algunos mamíferos, como los murciélagos, el esperma es mantenido vivo en el útero de la hembra y, de forma similar a lo que sucede en los peces, las cabezas de los espermatozoides mantienen una fuerte asociación con el epitelio uterino. Las hembras de mamíferos como algunos marsupiales forman paquetes de mucosas o bulbos (conjuntos celulares rodeados de secreciones) en donde almacenan el esperma.
Mantenerlos vivos
Los espermatozoides son células que requieren muchos cuidados, el ambiente que exigen para sobrevivir hace que gran parte de los animales no puedan almacenar esperma y sólo grupos selectos dentro del reino animal tienen las condiciones adecuadas. Dentro del aparato reproductor masculino se encuentran los tubos seminíferos, allí los espermatozoides están acumulados y nadando en un líquido que los nutre, rico en proteínas y azúcares; estos componentes seminales no están presentes en ninguna parte del aparato reproductor de la hembra, por lo que debe haber algo más que los mantenga con vida en lugares especializados de almacenamiento en el sistema reproductor femenino de las especies mencionadas.
Algunas de las pistas sobre la relación que existe entre el tejido de las espermatecas y los espermatozoides se han encontrado en ciertas salamandras. Los investigadores Boisseau y Jolie encontraron en 1994 que existe la secreción de glicoproteínas (proteínas más moléculas de carbono, hidrógeno y oxígeno) en el epitelio de las espermatecas que ayuda a mantener vivos a los espermatozoides, y en ese mismo año Guex señaló que es necesario un ambiente rico en zinc para el almacenamiento de esperma en mamíferos. Mediante algunas técnicas de laboratorio se han detectado polisacáridos (moléculas de carbono), lípidos (moléculas de grasa) y glucógeno (molécula de reserva energética formada por cadenas de glucosa) en los epitelios que están en contacto con el esperma y que ayudan a la nutrición y mantenimiento de los espermatozoides. También se ha investigado sobre la acción de hormonas como la progesterona (sustancia producida por las hembras) y la importancia de su participación en estos sitios de almacenamiento en aves y lagartijas.
¿Qué tan importante es?
Se ha relacionado el almacenamiento de esperma con otros aspectos de la vida de los organismos, como la duración de su ciclo de vida, la necesidad de migrar y los cambios ambientales que experimentan en diferentes estaciones del año. Los machos, por ejemplo, pueden dedicar pocos meses a los apareamientos con las hembras e invertir sus energías para otras actividades el resto del año; mientras la hembra se dedica a fecundar sus óvulos a lo largo del año con el esperma almacenado, con lo que maximiza la cantidad de crías que puede producir en ese año. Este tipo de estrategia reproductiva es característica de ciertos mamíferos (como algunos marsupiales) y varias aves marinas.
Una de las ventajas más interesantes de la retención de esperma es cuando hay diferencia en la vida media de las parejas, es decir, si la hembra vive por mucho tiempo y los machos poco, como es el caso de la temible viuda negra que, usando los espermatozoides de los ex pretendientes que se comió, puede fecundar sus huevos incluso años después.
Otra ventaja es que la hembra, al almacenar esperma de varios machos, amplia la variedad genética de su progenie pues hijos con genes de distintos padres pueden ser una buena estrategia en ambientes y condiciones cambiantes o desfavorables; los hijos de los padres más aptos sobrevivirían.
Increíblemente, en algunos animales se ha encontrado retención de esperma aun cuando las hembras no están sexualmente maduras; es el caso del tiburón Mustelus antarcticus y de la mosquita de la fruta Drosophila melanogaster. Se puede decir que los machos no pierden el tiempo y tratan de que sus espermatozoides sean los primeros en ser utilizados aun cuando la hembra sea demasiado joven.
¿ Y el ser humano?
El esperma humano sólo puede durar en las mujeres alrededor de siete días y en realidad no se le puede llamar almacenaje, sino que es simplemente el tiempo que los espermatozoides pueden resistir en el ambiente hostil de la vagina. La información resultó de un experimento en laboratorio con espermatozoides colocados en condiciones similares a las de la vagina, en las que sobrevivieron alrededor de una semana, demostrando solamente que siete días es el tiempo de vida promedio de los espermatozoides y no un tipo de almacenamiento de esperma.
|
||||||||||||||
|
Referencias bibliográficas
Holt, W. V. y R. E. Lloyd. 2010. “Sperm storage in the vertebrate female reproductive tract: how does it work so well?”, en Theriogenology, vol. 73, núm. 6, pp. 713-722.
Martínez Torres, Martín. 2009. “Almacenamiento de espermatozoides en la vagina de la lagartija vivípara Sceloporus torquatus (Sauria: Prhynosomatidae)”, en Acta Zoológica Mexicana, vol. 25, núm. 3, pp. 497-506.
Suárez, Susan. 2008. “Regulation of sperm storage and movement in the mammalian oviduct”, en The Intenational Journal of Developmental Biology, vol. 52, pp. 455-462.
Orr, Teri J. y Marlene Zuk. 2012. “Sperm storage”, en Current Biology, vol. 22, núm. 1, pp. 8-10.
|
||||||||||||||
| _______________________________________________ | ||||||||||||||
| Claudia Olivera Tlahuel José Jaime Zúñiga Vega Maricela Villagrán Santa Cruz Facultad de Ciencias, Universidad Nacional Autónoma de México. Norma Angélica Moreno Mendoza Instituto de Investigaciones Biomédicas, Universidad Nacional Autónoma de México. |
||||||||||||||
| _________________________________________________ | ||||||||||||||
|
cómo citar este artículo →
Olivera Tlahuel, Claudia; José Jaime Zúñiga Vega, Maricela Vallagrán Santa Cruz y Norma Angélica Moreno Mendoza. 2016. Almacenamiento de esperma, ¡las hembras lo hacen! Ciencias, núm. 120-121, abril-septiembre, pp. 30-33. [En línea].
|
||||||||||||||
 |
|
|||||||||||||||||||
| Carla G. Muñiz Irigoyen y Raúl Gío Argáez |
||||||||||||||||||||
|
No se puede interpretar muestras de poblaciones de maíz de manera eficiente sin conocer lo más que se pueda sobre la gente que ha cultivado ese maíz.
Edgar Anderson
|
||||||||||||||||||||
|
Los corales son animales minúsculos llamados pólipos,
en cuyos tejidos existe una población de algas llamadas zooxantelas, que viven en asociación simbiótica con ellos: el pólipo provee protección a las algas y éstas proporcionan alimento y oxígeno al coral. Cada coral secreta un esqueleto calcáreo duro alrededor de sí mismo; a medida que crecen, se dividen y forman colonias. Las colonias de coral se acumulan gradualmente, unas sobre otras (cada una puede alcanzar hasta mil años de edad), formando un arrecife de coral. Los arrecifes coralinos son ecosistemas marinos tropicales formados por organismos llamados hermatípicos o constructores arrecifales (los polipos), los cuales, mediante secreciones de carbonato de calcio, contribuyen a su formación, constituyendo comunidades de una gran biodiversidad, energéticamente autosuficientes. De todos ellos, los corales son el grupo de organismos más importante por ser la principal fuente de carbonatos y también por sus demandas fisiológicas, que son las que determinan los límites de distribución de los arrecifes, confinándolos a aguas de gran transparencia, con muy baja cantidad de sedimentos en suspensión y temperatura elevada, en general circunscritas a los trópicos. La transparencia está asociada con las necesidades fotosintéticas de las zooxantelas, mientras la temperatura lo está con los procesos de alimentación y reproducción de los propios corales y la simbiosis con las zooxantelas. El sedimento en suspensión afecta los corales al depositarse directamente sobre ellos e interferir en su alimentación y obstaculizar el proceso de fotosíntesis de las zooxantelas.
El arrecife de coral es uno de los ecosistemas más productivos y diversos del planeta. Además de los servicios ambientales que proporciona, es fuente de recreación y estimula el turismo y la economía del país en donde se encuentra. Los arrecifes coralinos son lugares con una gran importancia ecológica y se les conoce como hábitats críticos por su diversidad de funciones; desempeñan un papel muy importante en la dinámica costera al prevenir la erosión y disminuir la fuerza del oleaje, constituyendo la estructura de protección más efectiva contra el fuerte efecto de las tormentas tropicales y huracanes. Son lugares de crianza, refugio, alimentación y reproducción de muchas especies de invertebrados y vertebrados, principalmente de especies de carácter comercial, dando alimento a una gran parte de la población mundial. Todos estos organismos tienen una participación fundamental en el ecosistema, algunos como productores primarios, constructores del mismo arrecife, filtradores y depredadores.
Las diferentes expresiones que la comunidad coralina tiene a nivel local reflejan por tanto no sólo el resultado de las interacciones ecológicas del presente, sino también un complejo componente histórico, independientemente de que una comunidad compleja tenga diferentes vías de integración.
Los arrecifes se encuentran al interior de una franja delimitada por el trópico de Cáncer y el de Capricornio, generalmente del lado oriental de los continentes, lo cual se debe a que los grandes sistemas fluviales desembocan en las costas oeste de los continentes arrastrando sedimentos que enturbian las aguas.
A nivel mundial se considera que la Gran Barrera Arrecifal, ubicada en la costa oriental de Australia, y los arrecifes aledaños del sureste asiático constituyen el sistema arrecifal más relevante, tanto por su tamaño como por su riqueza de especies. El segundo sistema arrecifal de mayor importancia global se encuentra frente a las costas de Belice, en conjunto con los arrecifes de Quintana Roo, en México, Honduras y Guatemala. El sistema arrecifal del mar Rojo es uno de los más visitados, pero no es comparable en tamaño o estado de conservación con los ya mencionados. Los diferentes tipos de arrecifes coralinos se enlistan en el cuadro 1.
El área estimada que ocupan los arrecifes en México es de aproximadamente 1 780 km2. Comúnmente, los arrecifes pueden existir apenas a unos pocos centímetros de la superficie hasta cincuenta metros de profundidad. Los de la costa del Pacífico son considerados como parches arrecifales y se localizan en el Golfo de California (isla Carmen, isla Espíritu Santo y Cabo Pulmo), Roca Alijos, isla María Magdalena de las islas Marías e isla Clarión del archipiélago de Revillagigedo; también en las costas de los estados de Sonora, Sinaloa, Nayarit, Colima, Jalisco, Michoacán, Guerrero y Oaxaca (Puerto Escondido). Algunos de ellos se encuentran dentro del Sistema Nacional de Áreas Protegidas en diversas modalidades. En el Golfo de México existen áreas protegidas como el Parque Nacional Arrecifes de Veracruz, y el Parque Nacional de Arrecife Alacranes en Yucatán. En el Caribe se cuenta con cinco áreas naturales protegidas que implican ecosistemas marinos, la mayoría de ellos arrecifales: isla Contoy, costa occidental de Isla Mujeres, Punta Cancún y Punta Nizuc, Cozumel, Sian Ka’an y el banco Chinchorro, en sus modalidades de Parque Nacionales, Reservas de la Biósfera o Reservas Especiales. En esta última zona se encuentra el Sistema Arrecife Mesoamericano, complemento marítimo de 1 000 km2 de longitud en el Corredor Biológico Mesoamericano que comprende cinco estados de México (Campeche, Chiapas, Quintana Roo, Tabasco y Yucatán) y siete países centroamericanos, (Guatemala, Belice, Honduras, El Salvador, Nicaragua, Costa Rica y Panamá) iniciando en el cabo Catoche en Quintana Roo y terminando en las Islas de la Bahía en Honduras.
Pasado y presente
Los organismos productores de carbonatos han sido diferentes a lo largo del tiempo geológico y los arrecifes de coral actuales son muy diferentes de los del pasado. Desde el punto de vista geológico, un arrecife es una estructura carbonatada con relieve y límites laterales bien definidos, resultado de organismos fósiles unidos entre sí, ya sea porque son coloniales o porque estaban cementados, por lo cual un arrecife no está formado estrictamente por corales. A los organismos formadores de arrecifes se les llama bioconstructores.
Las construcciones de tipo arrecifal se encuentran presentes en la Tierra desde hace unos 3 500 millones de años, cuando aparecieron las microbialitas (depósitos sedimentarios orgánicos carbonatados) producto de cianobacterias (organismos fotosintetizadores primitivos que formaban tapetes algales), ésta fue la construcción arrecifal dominante hasta hace 600 millones de años. Los estromatolitos son el resultado de estos tapetes algales y los sedimentos, éstos aún están presente en algunas zonas relictuales como son la bahía Shark en Australia y en la Isla Stocking en las Bahamas. En México están presentes en Cuatro Ciénegas, Coahuila, y en Quintana Roo.
Durante la radiación cámbrica surgió una gran cantidad de organismos; hace aproximadamente 530 millones de años, las construcciones arrecifales estaban formadas por arqueociáticos (organismos parecidos a las esponjas), estromatolitos y algas calcáreas. Desde el Cámbrico medio (hace 509 millones de años) hasta el Devónico medio (hace 350 millones de años) los arrecifes estuvieron formados por una asociación de algas, esponjas y corales; estos últimos eran rugosos y tabulados, mientras las esponjas eran del tipo estromatopórida. Todos estos organismos están actualmente extintos. Posteriormente, del Devónico tardío (hace 350 millones de años) al Triásico temprano (hace 220 millones de años) los arrecifes estuvieron formados por corales, algas y briozoarios. A partir del Triásico (hace 220 millones de años) los arrecifes estuvieron formados por corales muy semejantes a los actuales, y en el Cretácico (145 millones de años) por rudistas (moluscos de dos valvas). A partir de finales del Cretácico (hace 65 millones de años) es cuándo empieza la historia geológica de los arrecifes de tipo coralino.
Los arrecifes tal como los conocemos en la actualidad están formados por corales y algas, que son organismos coloniales y sésiles (no pueden moverse), los cuales forman estructuras duras que resisten el oleaje. En términos del proceso de desarrollo de un arrecife moderno, existen dos componentes temporales principales: uno de largo plazo, determinado por la historia geológica de una localidad, y otro de mediano plazo, que resulta de cambios en la estabilidad climática y las tasas de ascenso del nivel del mar que se presentaron en el Holoceno (hace 7 000 o 5 000 años).
En la organización de la comunidad coralina que en la actualidad habita en la formación arrecifal interviene una multitud de interacciones ecológicas cuya temporalidad se estima en decenas de años y que reflejan en mayor o menor medida los determinantes geológicos que afectan la estructura arrecifal. También hay factores externos al sistema que tienen un papel importante en el desarrollo y mantenimiento de la estructura comunitaria y del propio arrecife coralino, como la cantidad y calidad de aportes terrígenos por descargas continentales o insulares; la interacción física y de intercambio de materiales y energía entre ecosistemas costeros tropicales (manglares, seibadales); y la frecuencia y magnitud de ciclones y tormentas tropicales. Hasta la fecha, sin embargo, es difícil evaluar (excepto en situaciones catastróficas) la importancia real que estos factores externos tienen en cada caso específico.
A pesar de lo anterior, muchos linajes individuales de corales han persistido en estos escenarios catastróficos y les ha tomado millones de años a los ecosistemas de arrecifes de coral restablecerse por sí mismos después de eventos de extinciones masivas. Estos patrones de geológica demuestran el potencial de los ecosistemas arrecifales y son importantes para evaluar el riesgo de extinción de las especies.
Alarma por su degradación
Además de brindar protección y seguridad a diversas especies, los arrecifes coralinos ayudan también a la generación de oxígeno en el planeta, mejorando los hábitats marinos. No obstante, las actividades humanas han transformado el ambiente; la susceptibilidad de los corales a estos procesos es variada debido a las diferencias morfológicas; por ejemplo, las especies ramificadas son más propensas a ser dañadas por las tormentas y por la presencia de buzos, mientras que las especies masivas incrustadas son más vulnerables al sobrecrecimiento de las algas.
La capacidad para recuperarse también es variable; su regeneración es energéticamente costosa y las especies difieren en la distribución de recursos, en la regeneración y otros procesos demográficos. Los sistemas arrecifales son frágiles y su reproducción es muy lenta, por lo que en todo el mundo afrontan inmensas presiones por las actividades humanas. El Programa de las Naciones Unidas para el Medio Ambiente estima que en los últimos treinta años se ha perdido casi 70% de los arrecifes de coral del mundo. Además del impacto que está teniendo el cambio climático pues al subir la temperatura del agua se ha disparado un gran número de enfermedades causantes de la pérdida de corales.
Debido a que la recuperación de arrecifes es un proceso muy lento, una vez removida la causa de afectación existen alternativas para ayudar a acelerar el proceso de recuperación. Entre ellas se encuentran las actividades de restauración, rehabilitación o remediación y conservación o preservación mediante el manejo de los recursos naturales, resultado de los numerosos estudios efectuados al respecto.
Para realizar una restauración debe tomarse en cuenta el tipo de ecosistema, la región, los antecedentes del sitio, precisar la causa y la escala del daño. Sólo así es posible evaluar las técnicas de restauración que pueden usarse para acelerar la recuperación de los arrecifes impactados, siempre apoyándose en los procesos naturales.
Debido a la degradación escalonada de los arrecifes de coral por la actividad humana, es muy importante entender los procesos asociados con el daño y la regeneración en los corales desde la perspectiva del manejo de los ecosistemas, tomando en cuenta que para ello se requieren grandes esfuerzos, al igual que para su conservación, además de una modificación de las políticas actuales. Por lo tanto, el éxito en la restauración también dependerá de los costos, las fuentes de financiamiento y la voluntad política de las instituciones interesadas en ella, pero ante todo de la colaboración y participación de las comunidades locales en los proyectos.
La restauración de arrecifes coralinos es un tema nuevo que puede ayudar al mejoramiento de estos ecosistemas. Un grupo internacional de científicos asociados a la National Oceanic and Atmospheric Administration ha creado diferentes programas para la restauración de los arrecifes y ayudar a reforzar las poblaciones silvestres; es así que los viveros de coral están surgiendo como un arma de buena fe en la lucha para preservar el ecosistema oceánico.
Estas técnicas crean beneficios tales como el aumento en la cobertura coralina, la recuperación del arrecife para la protección de organismos que viven en él, el incremento de las especies del mismo y la producción de oxígeno generado a partir de la fotosíntesis que realizan las algas que se encuentran en él, ayudando así a satisfacer la demanda de oxígeno del planeta por la creciente producción de dióxido de carbono provocado por los altos consumos de energía y la producción de gases de efecto invernadero en la atmósfera, además de que sirve como un atractivo para el turismo.
Los viveros de coral son un fenómeno relativamente nuevo. Los primeros intentos serios llegaron a mediados de la década de los noventas por obra del biólogo marino Baruch Rinkevich de la Universidad de Haifa en Israel. El laboratorio Rinkevich trabaja actualmente con sesenta especies de coral en setenta localidades de países como Jamaica, Colombia, Tailandia y Seychelles.
La restauración en arrecifes de coral ha despertado el interés de todos, ya que no sólo los investigadores han trabajado en las técnicas, sino también asociaciones civiles, organizaciones mundiales, habitantes y prestadores de servicios turísticos de las zonas costeras, además de los amantes de la acuariofilia y los grandes acuarios del sector privado, que también han contribuido considerablemente al conocimiento del cultivo de corales aprovechando los saberes de la acuicultura.
Algunas iniciativas
Como podemos darnos cuenta, hay muchas formas de proteger los arrecifes. El hecho de ser declarados Áreas Naturales Protegidas es favorable para que su cuidado y conservación sea más fácil, pero con ayuda de las leyes y normas que las protegen es mucho más sencillo realizar la tarea de conservación y aprovechamiento; sin embargo, la desaparición de los arrecifes es una realidad, ya que el cambio climático global, entre otros factores, parecen acelerar los procesos destructivos y minimizar los esfuerzos para la conservación de las especies, por lo que definitivamente debemos ser más conscientes de nuestras acciones y ayudar a crear y difundir los programas educativos en materia de conservación y manejo de los recursos naturales.
La Iniciativa Internacional para los Arrecifes de Coral (icri, por sus siglas en inglés) fue lanzada en 1994 con el objetivo de buscar soluciones al rápido deterioro de los arrecifes de coral en el mundo. En ella cooperan gobiernos, organizaciones no gubernamentales y organizaciones tales como el Programa de las Naciones Unidas para el Medio Ambiente, que auspician y promueven proyectos de investigación y educación sobre los arrecifes de coral en todo el mundo, en asociación con la Red Mundial de Monitoreo de los Arrecifes de Coral, la Alianza para los Arrecifes de Coral, la Red Internacional de Información sobre los Arrecifes de Coral, el Centro Mundial de Pesca, la Secretaría de la Iniciativa Internacional para los Arrecifes de Coral, el Instituto de Recursos Mundiales. Mediante los Programas de Mares Regionales y la Red Internacional de Acción para los Arrecifes de Coral se estableció una red mundial de “sitios demostración” con funcionamiento activo que sirven como modelo de Gestión Integrada de las Zonas Costeras y de las Áreas Marinas Protegidas para la aplicación de mejores prácticas de gestión, la cual cuenta con la participación activa de las comunidades locales, también apoyadas por el Convenio sobre la Diversidad Biológica, el Convenio Ramsar referente a los humedales de importancia internacional, la Comisión para el Desarrollo Sostenible y la Comisión Oceanográfica Intergubernamental. Por su parte, la Word Wild Foundation, está relacionada con los proyectos para la conservación del Sistema Arrecifal Mesoamericano.
En el Año Internacional del Arrecife 2008 se creó una campaña mundial al interior del programa de conservación de arrecifes de coral de la Administración Nacional Oceánica y Atmosférica con el fin de crear conciencia sobre el valor y la importancia de los arrecifes de coral y los tratados para su sustentabilidad, y motivar a la gente a proteger los arrecifes.
La educación sobre los arrecifes de coral y su importancia en la biósfera es una de las medidas de conservación y protección que se están promoviendo en diferentes partes del mundo. Es importante que todas las personas conozcan qué es un arrecife de coral y qué tipos hay. Si tienen la oportunidad de visitar un arrecife, es esencial que aprendan antes cómo comportarse y manejar sus movimientos en el agua para evitar dañar los corales.
Debemos también ser muy conscientes de las conexiones que existen entre los ecosistemas terrestres y los ecosistemas costeros. Muchas de las actividades humanas que impactan el arrecife de coral de manera negativa se originan tierra adentro y no necesariamente en el ambiente marino.
Los ecosistemas costeros como: manglares, praderas marinas, playas y arrecifes de coral están conectados entre sí por las corrientes marinas, el flujo de agua y de nutrimentos y por los organismos que se mueven entre ellos. La conservación, protección y buena salud ecológica de los arrecifes de coral depende de que los otros ecosistemas costeros se mantengan también saludables.
La clave del futuro ¿Hay esperanzas para los arrecifes de coral? Ésta es una pregunta que algunos investigadores han contestado con optimismo y la clave está en la evolución de las especies, ya que mediante los mismos experimentos o trabajos que se han realizado para la conservación y restauración de los arrecifes han surgido interesantes resultados que demuestran que los corales podrán resistir una siguiente extinción masiva debido al calentamiento global y a la acidificación de los mares adaptándose al cambio en las próximas décadas. Ciertamente, es una realidad que el clima cambia y el océano se acidifica y una posibilidad real que los arrecifes de coral como los conocemos podrían desaparecer; de modo que vale preguntarse ¿cómo serán los corales en el futuro?, ¿cómo sobrevivirán mientras otras especies no podrán?
Investigadores del Centro Oceanográfico Nacional de Southampton y la Universidad de Nueva York en Abu Dhabi, están comenzando a realizar estudios en los que seleccionan una característica específica de los corales del golfo Arábigo la cual facilitará en el futuro investigaciones a escala molecular y ver por qué ellos pueden soportar el calor estresante.
En un futuro marcado por el cambio climático, sólo los más fuertes o resistentes al calor sobrevivirán. Investigadores de la Universidad de Stanford están estudiando los procesos genéticos de cómo algunos corales serán capaces de soportar temperaturas inusuales, los cuales pueden ser la clave para la sobrevivencia de las especies en el mundo.
Otros investigadores, como Elena Couce y colaboradores, de la Universidad de Brístol, usando modelos computacionales para predecir los futuros cambios en la distribución global de los ecosistemas arrecifales bajo estos dos factores estresantes, encontraron que el mejor estado para los arrecifes de coral en las próximas décadas no será estar en los trópicos, sino en los subtrópicos.
Además, los investigadores marinos sugieren que es posible restaurar la cobertura viviente del coral de un sistema arrecifal degradado; sin embargo no es fácil, la composición de los arrecifes de coral continuará variando con el tiempo, con lo cual podría mantenerse la dominancia de los corales y sus asociaciones en un buen ecosistema y los servicios que presta. Los científicos podrían tomar ventaja de las oportunidades que los cambios causan a las variaciones naturales como un estímulo potencial para el beneficio del estado de los ecosistemas.
Para determinar el riesgo de extinción de los arrecifes de coral, los investigadores están examinando eventos pasados para poder vislumbrar cómo los corales actuales pueden pasar por el cambio climático. Se han encontrado fuertes relaciones entre las extinciones regionales pasadas y la vulnerabilidad de los corales modernos, sugiriendo que los eventos de extinción no son simplemente eventos casuales, pero que sí dependen de las características biológicas de las especies de coral.
Por otra parte, el trasplante de corales ya ha demostrado ser una solución simple y económica para la restauración de los arrecifes. Este proceso de restauración requiere muy poco entrenamiento, por lo que puede ser efectuado por buzos incluso como una actividad recreacional y educativa, adoptada por grupos de voluntarios de las comunidades. En tierra, las guarderías de coral están demostrando tener un tremendo potencial para la restauración. Los corales en las guarderías se van seleccionando y los más resistentes a las enfermedades, al calentamiento y los de crecimiento más rápido se van reintegrando al arrecife, dándose una “selección natural” de los organismos más fuertes y resistentes a los cambios que podrían enfrentar en un futuro cercano. Estudios realizados en 2013 por investigadores de varias universidades de Estados Unidos y Canadá sugieren que los corales están listos para adaptarse al calentamiento mediante una adaptación genética.
Por su parte, investigadores de la Universidad de Stanford han encontrado que algunos corales pueden rápidamente cambiar ciertos genes de modo que sobreviven en aguas más cálidas con temperaturas promedio mayores a 30 oC, ajustando sus funciones internas para tolerar aguas cincuenta veces más cálidas a las que ellos podrían llegar a adaptarse por sí solos mediante los cambios evolutivos.
Esto abre una nueva posibilidad para entender y conservar los corales. El objetivo es poner en marcha un programa de “evolución asistida por medios humanos” en el que se criarán corales resistentes en viveros controlados para su posterior plantación en zonas ya azotadas por condiciones cambiantes o en las que se anticipe tales tipos de cambios. Este método de creación de un “arrecife de diseño”, sin embargo, está sujeto a la controversia porque implica la alteración de los sistemas naturales.
En conclusión
Los arrecifes de coral son una parte importante del ecosistema global y han sido sujetos a un amplio espectro de daños a lo largo de su historia geológica, lo que ha originado extinciones masivas recurrentes. Los ecosistemas arrecifales actuales son un producto de tan sólo 45 a 50 millones de años de evolución. Durante este periodo los disturbios en los arrecifes de coral han variado desde pulsos de menor rango, tales como el pastoreo y la depredación, a grandes eventos infrecuentes, como picos de poblaciones de depredadores, huracanes y el incremento en la temperatura del mar, lo cual ha ocurrido en diferentes lapsos, frecuencia y distribución espacial, afectando los regímenes de disturbios naturales en los arrecifes de coral.
La conservación de muchos de los ecosistemas (terrestres, marinos y acuáticos continentales) es prioritaria para asegurar el futuro de las siguientes generaciones. Sin los servicios ambientales que brindan ecosistemas como los arrecifes coralinos, el bienestar de la sociedad y el crecimiento nacional estarán seriamente comprometidos.
|
||||||||||||||||||||
|
Referencias Bibliográficas
Barshis, Daniel J. et al. 2013. “Genomic basis for coral resilience to climate change”, en pnas, vol. 110, núm. 4, pp. 1387-1392.
Couce, Elena, Andy Ridgwell y Erika J. Hendy. 2013. “Future habitat suitability for coral reef ecosystems under global warming and ocean acidification”, en Global Change Biology, vol. 19, núm. 12, pp. 3592-3606. Graham, Nicholas A. J. et al. 2013. “Managing resilience to reverse phase shifts in coral reefs”, en Frontiers in Ecology and the Environment, vol. 11, núm. 10, pp. 541-548. Ramos Esplá, A. A. 2002. “Arrecifes artificiales como medidas de restauración de hábitats marinos costeros”, en Ecosistemas, vol. 11, núm. 1, pp. 64-69. En la red gl/bMqMu6 goo.gl/mG2SHd |
||||||||||||||||||||
| _____________________________ |
||||||||||||||||||||
| Carla G. Muñiz Irigoyen Instituto de Ecología, Universidad Nacional Autónoma de México. Es maestra en ciencias biológicas con orientación en restauración ecológica, egresada de la Facultad de Ciencias, UNAM. Raúl Gío Argáez Instituto de Ciencias del Mar y Limnología, Universidad Nacional Autónoma de México. Es doctor en ciencias y decano de los profesores de paleontología de la Facultad de Ciencias, UNAM. También es investigador responsable del laboratorio de micropaleontología ambiental en el Instituto de Ciencias del Mar y Limnología de la misma institución. En 2007 fue designado Socio Honorario de la Real Sociedad Española de Historia Natural. |
||||||||||||||||||||
| _____________________________ | ||||||||||||||||||||
|
cómo citar este artículo →
Muñiz Irigoyen, Carla G. y Gío Argáez, Raúl. 2016. Conservación y restauración en arrecifes de coral. Ciencias, núm. 120-121, abril-septiembre, pp. 60-71. [En línea].
|
||||||||||||||||||||
 |
|
||||||||||
| James Enrique González Flores, Geovani López Ortiz y María Alicia González Manjarrez |
|||||||||||
|
En sentido estricto,
nada en la evoluci{on se crea de nuevo,
los genes surgen de genes preexistentes..
Susumu Ohno
|
|||||||||||
|
Se entiende por duplicación génica el aumento en el número
de genes a partir de secuencias preexistentes, y tales duplicaciones pueden comprender unos cuantos nucleótidos, genes, fragmentos de cromosomas, cromosomas e incluso genomas completos. La historia de su estudio se remonta a principios del siglo pasado, cuando en 1911 el botánico Yoshinari Kuwada encontró que uno de los cromosomas del maíz se encontraba duplicado. Posteriormente, en 1918, Calvin Bridges consideró la posibilidad de que fragmentos redundantes de cromosomas pudieran modificarse a lo largo del tiempo y llevar a cabo funciones distintas a las que desarrollaban originalmente. En 1932, el genetista John Burdon Haldane, en su libro Las causas de la evolución, propone que los eventos de duplicación génica podrían influir en la evolución de los organismos, en ese sentido, especies con más de una copia de un gen serían menos propensas a posibles efectos perjudiciales de mutaciones sencillas pues éstas se repartirían entre las diversas copias existentes. En 1970, Susumu Ohno publicó su libro Evolution by gene duplication, en el que estableció la importancia de la duplicación génica en la evolución de las especies. Sin embargo, fue hasta la década de los noventas cuando gracias al enorme auge que adquirió la secuenciación de genomas completos se encontró que la duplicación de genes era abundante en todos los organismos. En la actualidad se ha determinado que la gran mayoría de las especies presentan un alto porcentaje de genes duplicados, y se considera que la duplicación constituye una de las principales fuentes de variación genética; es por lo tanto un elemento clave en la generación de la diversidad biológica (figura 1).
El origen de los genes duplicados ¿Cómo surgen nuevos genes y qué repercusión tienen en la fisiología de los organismos? Ésta es una de las preguntas más importantes que se ha planteado la genética molecular y cuya respuesta se encuentra justamente en el estudio de los genes duplicados o genes parálogos, los cuales pueden originarse mediante los siguientes procesos: a) entrecruzamiento de regiones homólogas del genoma o crossing over, que suele generar genes repetidos en “tándem”, esto es, varios genes duplicados que se encuentran en posiciones adyacentes en el genoma —dependiendo del posicionamiento del entrecruzamiento, la región duplicada puede contener parte del gen, el gen entero o varios genes; b) retrotranscripción, que ocurre cuando un arn mensajero es retrotranscrito a adn complementario y después es insertado en el genoma, lo cual suele generar pérdida o ganancia de segmentos de adn, que pueden ser insertados e interrumpir de manera aleatoria cualquier secuencia del genoma; y c) duplicaciones cromosómicas o del genoma, que pueden ocurrir durante la división celular, después de la replicación del adn; un tipo de duplicación a gran escala, muy frecuente en plantas, pero rara vez se presenta en animales.
Destino evolutivo de los genes duplicados
Al término de la década de los setentas surgió un planteamiento importante sobre el destino evolutivo de los genes duplicados. El modelo de diversificación funcional sugerido por Ohno propone que los pares de genes duplicados evolucionan a diferentes velocidades, de suerte que una de las copias evoluciona lentamente, manteniendo la función original, mientras que la otra copia cambia rápidamente, adquiriendo con ello una nueva función. Este modelo ha sido analizado con gran detalle y se ha comprobado que tales escenarios únicamente se cumplen en ciertos casos. Un modelo alternativo conocido como duplicacióndegeneracióncomplementación establece que, dado que muchos genes pueden tener más de una función, después de una duplicación ambas copias p ueden mutar libremente, de manera tal que los dos genes que se han degenerado son necesarios para llevar a cab o la función ancestral, que realizaba el gen original antes de la duplicación.
En términos generales, los genes duplicados pueden tener cuatro posibles destinos evolutivos: 1) la conservación de la función ancestral, que ocurre cuando la dosis adicional representa una ventaja y se mantiene por conversión génica constante, y es común en genes que codifican para proteínas que forman complejos macromoleculares y en donde es importante mantener la estequiometría de las subunidades del complejo; 2) la pseudogenización, que es cuando una de las copias se pierde, ya sea porque acumuló mutaciones sobre su región regulatoria que impiden la expresión del gen o bien por mutaciones en la región codificante que imposibilitan la generación de un producto funcional —tras una duplicación génica, los procesos de pseudogenización son los que ocurren con mayor frecuencia, y en especies como Saccharomyces cerevisiae llegan a ser cerca de 90%; 3) la subfuncionalización, cuando ambos genes son necesarios para llevar a cabo la función original debido a que han acumulado mutaciones sobre la región codificante o regulatoria, es decir, la función que previamente llevaba un solo gen se repartirá entre las copias que resultan de tal duplicación —esta división de funciones tiene múltiples implicaciones y hay ocasiones en que sólo es evidente bajo un contexto metabólico peculiar; y 4) la neofuncionalización, cuando mutaciones a lo largo de la región regulatoria o codificante inciden directamente sobre los patrones de expresión o sobre las propiedades bioquímicas del producto, facilitando la adquisición de nuevas funciones —los procesos de neofuncionalización de proteínas regulatorias incluyen el surgimiento de nuevos sitios de unión al adn, y cuando los cambios ocurren sobre las secuencias regulatorias presentes en el adn, éstas pueden ser reconocidas por elementos que no afectaban al gen ancestral. La neofuncionalización propicia la modificación de aminoácidos que alterarán la especificidad, la afinidad o las propiedades cinéticas de las enzimas, así como el establecimiento de nuevas interacciones de proteínas debido a cambios en la secuencia codificante o de localización subcelular.
Un ejemplo de neofuncionalización en la naturaleza lo presentan los peces zoárcidos antárticos, que tienen la capacidad de sobrevivir a temperaturas cercanas a cero grados centígrados. Los ancestros de estos peces tenían un gen que codificaba para una enzima denominada ácido siálico sintasa; después de un evento de duplicación de este gen, una de las copias resultantes acumuló mutaciones que le permitieron codificar para una proteína que es secretada al exterior y cuya función ahora es evitar la formación de cristales de hielo, los cuales podrían ser fatales para estos peces; este hecho influyó de manera notoria en la adaptación de los mismos a ambientes fríos.
La importancia de la duplicación génica
La duplicación génica es un evento que está presente en los tres dominios del árbol de la vida: bacterias, arqueas y eucariontes, es decir, constituye una característica vigente y concurrente en todos los seres vivos (cuadro 1). Su importancia radica en tres postulados clave: 1) representa un mecanismo principal en la innovación de genes y de funciones asociadas a sus productos; 2) ha sido un factor determinante en el surgimiento y evolución de vías metabólicas y por lo tanto en el origen de los primeros seres vivos; y 3) la diversidad biológica es el resultado de múltiples procesos de duplicación génica, desde la duplicación de pequeños fragmentos de un gen, hasta de genes y genomas completos.
Como se mencionó, la mayoría de los genes duplicados pueden acumular mutaciones rápidamente hasta perder su función; sin embargo, una fracción pequeña pero importante de genes duplicados (10%) puede permanecer en el genoma y formar familias completas, esto es, grupos de genes que provienen de un mismo gen ancestral. La familia de la tripsina, presente en el genoma de la mosca Drosophila melanogaster, es una de las familias más grandes de genes parálogos constituida por 111 miembros. Otro caso interesante es la familia de genes parálogos que codifican para los receptores olfatorios en el ratón, la cual tiene cerca de 1 500 genes y se ha postulado que la mayoría de éstos emergieron a partir de unas cuantas copias ancestrales, mismas que a lo largo del tiempo se duplicaron de manera reiterada y generaron toda una gama de receptores con una mayor especificidad para el reconocimiento de los olores.
La robustez génica puede ser definida como: la habilidad que tiene un sistema biológico para resistir mutaciones y perturbaciones sin alterar su funcionamiento; esto puede ser propiciado por la redundancia génica, lo cual implica que los genes duplicados pueden balancear la pérdida de funciones de aquellas copias que reciben mutaciones que afectan directamente su función. La importancia de la robustez en un sistema biológico es que permite crear nuevas redes biológicas, rutas metabólicas y redes regulatorias alternativas; por lo tanto, la robustez permite la innovación evolutiva y la diversidad fenotípica.
Genes duplicados en la levadura de cerveza
El análisis de la secuencia genómica de la levadura Saccharomyces cerevisiae puso de manifiesto la existencia y la magnitud de la redundancia génica; alrededor de 30% de su genoma está constituido por genes presentes en más de una copia. Estos genes parálogos son el resultado tanto de una duplicación total del genoma, la cual involucró la pérdida y retención selectiva de algunos de ellos, así como de eventos independientes de duplicación génica a menor escala. El hallazgo permitió identificar un gran número de genes parálogos que codifican para enzimas implicadas en el metabolismo del carbono y del nitrógeno.
Nuestro grupo de investigación inició el estudio de la diversificación de genes y proteínas parálogas utilizando como modelo algunos pares de genes cuyos productos participan en la biosíntesis de aminoácidos en S. cerevisiae. La selección de tales genes está relacionada con enzimas que participan en la biosíntesis de aminoácidos y durante el metabolismo central del carbono (glucólisis y ciclo de los ácidos tricarboxílicos), por tanto su especialización podría resultar en el desarrollo de funciones importantes en la utilización de compuestos de carbono relacionados con la generación de energía como el adenosíntrifosfato o atp.
La levadura S. cerevisiae tiene la capacidad de crecer y generar energía en forma de atp en condiciones fermentativas o respiratorias (metabolismo facultativo). Se ha propuesto que la retención selectiva de genes parálogos facilitó la adquisición de un metabolismo facultativo en esta levadura, por tal motivo nuestro grupo se ha centrado en el estudio de la diversificación o redundancia de los genes parálogos, así como de sus productos. Para ello se analiza el papel de cada uno de los dos genes mientras la levadura se cultiva en condiciones fermentativas y respiratorias. Asimismo, hemos comparado la función de los genes parálogos de S. cerevisiae con la de los genes ortólogos presentes en otras especies denominadas “tipo ancestral”.
Algunas de las preguntas que se pretenden contestar al estudiar la función de los parálogos de la levadura son: ¿la duplicación de genes constituye una redundancia funcional?, ¿cómo diversifican los genes parálogos a lo largo de la evolución?, ¿qué mecanismos moleculares están involucrados en la diversificación funcional?, ¿cómo se diversifican las enzimas parálogas?, ¿qué ventajas adaptativas y fisiológicas representa el preservar tales genes duplicados?, ¿la conservación de genes parálogos constituyó una adaptación al metabolismo facultativo?
Entre las parejas de genes parálogos que nuestro grupo ha estudiado destacan genes implicados en la biosíntesis de aminoácidos tales como: GDH1/GDH3, LYS20/LYS21, BAT1/BAT2, ALT1/ALT2 y LEU4/LEU9, las cuales se conservaron después de la duplicación completa del genoma de S. cerevisiae. Éstos y los productos codificados se han estudiado utilizando metodologías que nos permiten establecer su función y compararla con la de los genes ortólogos de organismos tipo ancestral, un enfoque que nos permite determinar si la función tipo ancestral se ha conservado en los parálogos, si es redundante o se ha diversificado. El análisis se ha centrado en determinar las propiedades enzimáticas, la localización subcelular y las interacciones proteínaproteína en los parálogos, así como en su regulación transcripcional y la organización de su cromatina.
El caso que se ha estudiado con mayor detalle lo constituyen las proteínas parálogas GDH1/GDH3, las cuales asimilan nitrógeno y sintetizan glutamato a partir de amonio y cetoglutarato. En condiciones fermentativas, la formación de glutamato depende exclusivamente de la acción de GDH1, sin embargo, en condiciones respiratorias se requiere la expresión simultánea de GDH1/GDH3, lo que conlleva a la formación de isozimas heteroligoméricas para llevar a cabo su función en tales condiciones. Por lo tanto, la retención de dichos genes permite la formación de isozimas homohexaméricas (GDH1 y GDH3) y de isozimas heterohexaméricas en las que se combinan monómeros de GDH1 y GDH3. Cada una de las isozimas de esta familia tiene una capacidad peculiar de utilizar cetoglutarato, GDH1 posee la mayor capacidad, en tanto que GDH3 tiene una menor capacidad. El crecimiento óptimo en etanol depende de la presencia de enzimas heterohexaméricas de capacidad intermedia. En glucosa la expresión de GDH3 se reprime por remodelación de cromatina y por tanto la isozima prevalente en esta condición es la GDH1 homohexamérica, lo que permite que en esta condición las levaduras crezcan a una velocidad mayor a la observada en etanol.
Otro caso interesante es el de las isozimas homocitrato sintasa codificadas por los parálogos LYS20/LYS21, las cuales intervienen en el primer paso de la síntesis del aminoácido lisina. El análisis de estas enzimas parálogas demostró que se requieren ambas isozimas para poder crecer en condiciones fermentativas, es decir, en esta condición la función de LYS20 y LYS21 es redundante. Sin embargo, la diversificación de las propiedades cinéticas de las proteínas LYS20/LYS21 fue esencial para el metabolismo respiratorio, ya que en tal condición la biosíntesis de lisina depende exclusivamente de LYS21. La inhibición diferencial por lisina de cada una de las dos isozimas y la regulación de la concentración intracelular de cada isozima resulta en un delicado sistema regulatorio que coordina la eficiencia con la que el cetoglutarato se utiliza para la síntesis de lisina o para la síntesis de algún otro intermediario. Por lo tanto, la retención y diversificación funcional de LYS20 y LYS21 con papeles parcialmente redundantes ha contribuido a la adquisición del metabolismo facultativo.
Otro ejemplo lo ilustran las aminotransferasas de cadena ramificadas (BCAATs, por sus siglas en inglés), las cuales son codificadas por los parálogos BAT1/BAT2 y catalizan el primer paso de la biosíntesis y el último del catabolismo de los aminoácidos de cadena ramificada mediante la transferencia del grupo amino entre los aminoácidos valina, isoleucina y leucina y el ceto ácido correspondiente. Estudios recientes muestran que el único ortólogo KlBAT1 en la levadura tipo ancestral K. lactis es una enzima bifuncional que participa en la biosíntesis y el catabolismo de valina, isoleucina y leucina. Esta función dual ha sido distribuida en las proteínas parálogas BAT1/BAT2 de S. cerevisiae, apoyando el modelo de subespecialización que explica la evolución de los genes duplicados.
Hasta ahora, los resultados publicados han demostrado que la enzima ancestral distribuyó su función mediante la divergencia de expresión de BAT1/BAT2 y la localización subcelular diferencial de los productos. BAT1 se expresa en condiciones biosintéticas, mientras que BAT2 en catabólicas; BAT1 tiene una localización mitocondrial, mientras que BAT2 una localización citoplasmática. Este estudio demostró que la expresión diferencial y la localización subcelular de BAT1/BAT2 resultó en la distribución del papel biosintético y catabólico del gen tipo ancestral de K. lactis en dos isozimas que constituyen una adaptación al metabolismo facultativo.
Conclusiones
El estudio del destino evolutivo de algunos genes duplicados presentes en S. cerevisiae cuyos productos participan en la biosíntesis de aminoácidos indica que la retención y la diversificación de los mismos ha tenido un profundo impacto en la adaptación de la levadura S. cerevisiae al metabolismo facultativo, desempeñando un papel importante en la adquisición de un “nuevo” modo de vida que depende de la capacidad de crecer y obtener energía en condiciones fermentativas o respiratorias.
Agradecimientos
Al Consejo Nacional de Ciencia y Tecnología CB-2014-239492. Al Programa de Apoyo a Proyectos de Investigación e Innovación Tecnológica PAPIIT IN201015.
|
|||||||||||
|
Referencias Bibliográficas
Gu, Z. et al. 2002. “Extent of gene duplication in the genomes of Drosophila, nematode and yeast”, en Molecular Biology and Evolution, vol. 19, núm. 3, pp. 256-262. Levasseur, Anthony y Pierre Pontarotti. 2011. “The role of duplications in the evolution of genomes highlights the need for evolutionary-based approaches in comparative genomics”, en Biology Direct, vol. 6, pp. 1-12. Lilly, M. et al. 2006. “The effect of increased branched-chain amino acid transaminase activity in yeast on the production of higher alcohols and on the flavour profiles of wine and distillates”, en fems Yeast Research, núm. 5, pp. 726-743. Lynch, M. y J. S. Conery. 2003. “The origins of genome complexity”, en Science, núm. 302, pp. 1401-1404. _____. 2000. “The evolutionary fate and consequences of duplicate genes”, en Science, núm. 290, pp. 1151-1155. Mombaerts, Peter. 2001. “The human repertoire of odorant receptor genes and pseudogenes”, en Annual Review of Genomics and Human Genetics, vol. 2, pp. 493-510. Ohno, Susumu. 1967. Sex chromosomes and sex-linked genes. Springer, Berlín. Wolfe, K. H. y D. C. Shields. 1997. “Molecular evidence for an ancient duplication of the entire yeast genome”, en Nature, núm. 387, pp. 708-713. Zhang, J. 2003. “Evolution by gene duplication: an update”, en Trends in Ecology and Evolution, núm. 18, pp. 292-298. |
|||||||||||
| _____________________________ |
|||||||||||
| James Enrique González Flores Instituto de Fisiología Celular, Universidad Nacional Autónoma de México. Es biólogo por la Facultad de Estudios Superiores Iztacala y maestro en ciencias bioquímicas por la Facultad de Química de la UNAM; actualmente está por obtener el grado de doctor en el posgrado de Ciencias Bioquímicas de la misma casa de estudios. Geovani López Ortiz Instituto de Fisiología Celular, Universidad Nacional Autónoma de México. Es biólogo experimental por la Universidad Autónoma Metropolitana y doctor en ciencias bioquímicas por la Facultad de Química de la UNAM. Labora en la Subdivisión de Medicina Familiar en la División de Estudios de Posgrado en la Facultad de Medicina de la UNAM. María Alicia González Manjarrez Instituto de Fisiología Celular, Universidad Nacional Autónoma de México. Es bióloga por la Facultad de Ciencias de la UNAM y realizó su doctorado en investigación biomédica básica en la misma casa de estudios. Actualmente es investigadora del Instituto de Fisiología Celular de la UNAM, pertenece al Sistema Nacional de Investigadores (nivel III) y es jefa del Departamento de la División Académica de Ciencias Básicas, Bioquímica y Biología Estructural del mismo instituto. |
|||||||||||
| _____________________________ | |||||||||||
|
cómo citar este artículo →
González Flores, James Enrique; Geovani López Ortiz y María Alicia González Manjarrez. 2016. Duplicación génica, causas y repercusiones en los seres vivos. Ciencias, núm. 120-121, abril-septiembre, pp. 116-123. [En línea].
|
|||||||||||
 |
|
|||||||||||
| Elizabeth G. Pringle y Rodolfo Dirzo | ||||||||||||
|
Impulsado por el impacto antropogénico, el clima mundial está cambiando. La temperatura promedio de la superficie de la Tierra ha aumentado más de 0.5 ºC en los últimos cincuenta años. Los eventos extremos de precipitación, incluyendo huracanes y sequías, también hoy son más frecuentes que antes. Además, se altera la dinámica de las relaciones entre la disponibilidad de agua y la temperatura, de manera que el aire más caliente se satura más de agua, lo que conlleva a cambios en la cantidad de nubes con consecuencias climáticas a diferentes escalas espaciales. Todos estos cambios se deben a la acumulación de gases de efecto invernadero en la atmósfera, detonada a partir de la Revolución industrial en el siglo xix. Mientras más gases de efecto invernadero añadimos a la atmósfera —debido principalmente a nuestro uso de combustibles fósiles y a la expansión de las actividades agrícolas y ganaderas— más contribuimos a la manifestación del efecto invernadero y el planeta continuará su empinada trayectoria de calentamiento global o, más precisamente, de cambio climático antropogénico.
Tal vez la imagen más emblemática del cambio climático antropogénico es la de un oso polar, desolado, sobre un trozo de hielo que flota en el Ártico. Esta imagen es representativa por varias razones, entre ellas el que los diferentes modelos de circulación general consistentemente pronostican que los aumentos en la temperatura causados por el cambio climático antropogénico serán más intensos en latitudes mayores. Un efecto importante será el deterioro o pérdida directa del hábitat propicio de muchas especies con impactos severos, por ejemplo, los organismos adaptados al frío y al hielo permanente —aun en aquellos casos en los que pareciera que el hábitat es de gran extensión, como el del oso polar.
Sin embargo, es muy importante notar que los trópicos también estarán muy afectados por los cambios del clima. En un sentido geográfico, los trópicos no se restringen a las latitudes ecuatoriales, sino que se extienden hasta una latitud de aproximadamente 23º a ambos lados del ecuador, adonde el Sol llega directamente por lo menos una vez por año. En términos latinoamericanos, esa expansión geográfica consiste en toda la superficie ubicada aproximadamente entre la latitud del sur de Ciudad Victoria, en el norte de México, y la frontera entre Bolivia y Argentina, en el sur. Ya que los trópicos, particularmente aquellos de América Latina, contienen la mayoría de las especies en el planeta, los efectos del cambio climático antropogénico sobre la biodiversidad tropical serán graves, complejos y de repercusión global.
Al hacer referencia a cómo el cambio climático antropogénico afectará la biota del planeta, es común pensar primeramente en los efectos sobre la distribución de las especies, individualmente. Conforme a la teoría del nicho, cada especie de planta, animal y microorganismo está adaptada a vivir dentro de un marco de condiciones abióticas (de temperatura y disponibilidad de agua y características del suelo); es decir, el “nicho ecológico fundamental”.
Nicho fundamental y nicho realizado
Cuando cambian las variables abióticas del ambiente, una especie puede a) extinguirse, b) adaptarse a las nuevas condiciones o c) migrar a otro lugar donde las condiciones son más parecidas a las del nicho fundamental. Por ejemplo, las lagartijas, que son animales ectotermos y ajustan su temperatura corporal mediante desplazamientos dentro de su hábitat y por respuestas conductuales, tienen temperaturas críticas baja y alta que representan un umbral más allá del cual no pueden funcionar, así como una temperatura óptima para sus actividades. Es conocido que las temperaturas críticas y óptimas afectan la supervivencia de las lagartijas. De hecho, se pronostica que más de veinticuatro especies de lagartijas mexicanas del género Sceloporus estarían en riesgo de extinción hacia el año 2080, con riesgos especialmente altos para las especies adaptadas a vivir en la alta montaña, ya que esas especies no tendrán opciones de desplazarse a sitios con temperaturas que se ubican dentro del ámbito del nicho fundamental.
Además de las condiciones abióticas que definen el nicho fundamental, están las condiciones que surgen a partir del hecho de que las especies no viven en aislamiento, sino que su supervivencia y adecuación dependen también de otras especies. Dentro del nicho fundamental, una especie puede sobrevivir o no, dependiendo de la presencia o ausencia de otras especies, lo cual define el nicho (biótico) realizado. Esto es importante porque el cambio climático antropogénico también tendrá efectos importantes, si bien menos reconocidos, sobre las interacciones entre especies. Imaginemos que una especie de lagartija adaptada a las temperaturas de las tierras bajas emigra a una elevación más alta para mantener su temperatura óptima: ¿qué pasará con los insectos de los que se alimenta la lagartija?, ¿y qué le ocurrirá a las otras lagartijas que se alimentan de los mismos insectos?, ¿y qué le pasará a los depredadores de la lagartija?
Por medio de sus interacciones con la lagartija desplazada, las otras especies también tendrían que cambiar su conducta ecológica o su distribución. Es decir, ya que todas las especies en el mundo están involucradas en redes complejas de interacciones, los cambios en la distribución de una especie también afectará otras. Estos efectos pueden ocurrir por dos mecanismos no excluyentes: 1) cambios en la superposición de especies en las comunidades ecológicas y 2) cambios en los rasgos de las especies, los que a su vez modifican sus interacciones bióticas. Los cambios en las interacciones de las especies ocasionados por el cambio climático antropogénico también pueden causar mortalidad y extinción local o global de especies. Por ejemplo, cambios en el ritmo de floración de las plantas pueden dejar a los insectos polinizadores sin fuentes de alimentación. Además, se ha propuesto que las interacciones de las especies son más importantes en los trópicos que en otras latitudes en términos de frecuencia, diversidad y efectos sobre la adecuación. Esto sugiere que los impactos del cambio climático antropogénico sobre las interacciones bióticas que definen el nicho realizado de muchas especies serán especialmente importantes en las regiones tropicales.
Veamos un ejemplo hipotético, una especie de lagartija es restringida a ciertas condiciones abióticas determinadas por la disponibilidad de agua y temperatura, o sea, a su nicho fundamental. Sin embargo, sus presas preferidas (chapulines y escarabajos) sólo se encuentran en una parte del nicho fundamental, así que antes del cambio climático antropogénico (a la izquierda de la línea puntada de la figura) la lagartija sólo se encuentra donde las condiciones abióticas y bióticas coinciden, o sea, en su nicho realizado. Cuando cambia el clima y la lagartija migra (a la derecha de la línea puntada), los escarabajos ya no se encuentran dentro del nicho fundamental de la lagartija, y su nicho realizado se restringe.
¿Temperatura o agua?
La mayoría de los estudios ecológicos de los efectos del cambio climático antropogénico se enfoca en los aumentos de temperatura. Aunque, en términos absolutos, éstos serán mayores en latitudes más altas, es muy probable que los aumentos relativos serán más graves para las especies tropicales. Esta observación deriva de la famosa hipótesis del ecólogo Daniel Janzen, quien propone que los pasos de montaña son más altos en los trópicos. La propuesta no es que los pasos son literalmente más altos, sino que son relativamente más altos porque las especies tropicales típicamente experimentan menos variación térmica anual que las especies templadas, las cuales afrontan las condiciones de un invierno muy frío tras un verano muy caliente, oscilaciones térmicas a las que se han adaptado en tiempo evolutivo. Así, en contraste con las especies de altas latitudes, cruzar un paso de montaña para una especie tropical involucra afrontar condiciones de un clima al que no está adaptada y en el cual no puede sobrevivir. La adaptación de las especies tropicales a un nicho climático angosto puede ser una de las razones que explica la existencia de más especies en los trópicos. Aplicando la misma lógica a las reacciones de las especies tropicales cuando se enfrentan al calentamiento global, se puede colegir que los efectos serán más graves para las especies tropicales porque están adaptadas a nichos térmicos muy angostos.
A pesar de la importancia evidente de la temperatura, es posible que los cambios en la cantidad y estacionalidad de la precipitación en los trópicos tendrán aún más impacto en la biodiversidad tropical. Desafortunadamente, las predicciones de los cambios futuros de precipitación son menos precisos en general que las predicciones de los cambios de temperatura. Es difícil entonces definir un patrón de los cambios en la cantidad anual de precipitación y cómo afectarán a las especies. Es quizás aún más difícil incluir medidas de la distribución temporal de las lluvias, las cuales pueden ser muy importantes para las especies adaptadas a la estacionalidad. La importancia biológica de los patrones de precipitación en los trópicos fue notada hace mucho tiempo por Alexander von Humboldt, el gran naturalista y explorador alemán que viajó extensamente por América Latina a principios del siglo xix. Humboldt observó que aunque el clima de los trópicos parece más estable que el de las zonas templadas por la falta de invierno, la estacionalidad de precipitación en los trópicos es muy importante. Por ejemplo, propuso que la sequía anual en Amazonía causa grandes migraciones de aves. Más tarde, hacia la mitad del siglo xx, el biólogo evolutivo y genetista Theodosius Dobzhansky argumentó que el agua es el factor limitante para la vida tropical, si bien es reconocido que la disponibilidad lumínica es también muy importante en las zonas de selvas perennifolias.
No obstante los pocos estudios disponibles sobre el efecto de los cambios en la disponibilidad hídrica en las interacciones de especies tropicales, la información existente subraya su importancia. Uno de los ejemplos más prominentes argumenta que los cambios hidrológicos son responsables del aumento en la infección por el hongo quítrido que ha devastado a los anfibios. Las extinciones recientes de sapos arlequín del género Atelopus spp. se atribuyen a una combinación fatal del hongo y el cambio climático antropogénico. El hongo quítrido (Batrachochytrium dendrobatidis) fue descubierto en el año 1993 como un patógeno de ranas en Australia. Al principio los biólogos pensaron que el hongo podría ser limitado por el calentamiento global porque prospera mejor en condiciones frías que en condiciones relativamente más calientes. Se dejaba de lado la conexión crucial entre el aumento en la temperatura y la disponibilidad de agua. Un grupo de investigadores notó, ciertamente, que la proporción de días nublados había aumentado en los últimos cuarenta años en los bosques mesófilos de Costa Rica, lo cual implica que la temperatura del día disminuye mientras que la de la noche aumenta. Desafortunadamente, éstas son las condiciones perfectas para el desarrollo del hongo quítrido, lo cual a su vez coincide con la resonada extinción de sapos del bosque mesófilo tropical.
Un ejemplo más del efecto de los cambios en la disponibilidad de agua viene de otro hábitat tropical muy afectado por la precipitación: los bosques secos caducifolios. Estos bosques, antes ampliamente distribuidos por las regiones tropicales, ahora están muy amenazados debido a la facilidad con la cual se convierten, por medio de incendios, en campos de cultivo y ganadería. Este hábitat se caracteriza por una época seca anual muy marcada, una fuerte estacionalidad que afecta a todas las especies y por lo tanto sus interacciones bióticas. En uno de los pocos ejemplos empíricos del efecto posible de los cambios hidrológicos en las especies del bosque seco, se investigó el efecto de la variación de las lluvias en la adecuación de pericos de cabeza lila dentro un bosque caducifolio mexicano, descubriéndose que la cantidad de lluvia de años anteriores estaba correlacionada positivamente con la cantidad de huevos que ponen las aves y las tasas de éxito de las crías. Estos efectos probablemente están mediados por la mayor disponibilidad de frutos de los que se alimentan los pericos después de años más húmedos. Así, la cantidad de lluvia en el bosque seco caducifolio tiene efectos directos sobre el éxito reproductivo de las plantas y a su vez efectos indirectos sobre el éxito reproductivo de los pericos.
Usar el pasado para entender el futuro
¿Cómo podemos pronosticar los efectos del cambio climático antropogénico sobre las interacciones de las especies? Una estrategia es estudiar el pasado. Durante el transcurso del tiempo geológico de la Tierra han ocurrido muchos cambios del clima que tuvieron efectos importantes, a veces catastróficos, para las especies del planeta. Usando métodos de la geología es posible explorar posibles correlaciones entre las temperaturas del pasado con patrones en la diversidad de especies antiguas.
Es posible estimar la temperatura de tiempos antiguos mediante la proporción entre los isótopos de oxígeno pesado y ligero que se encuentran en las rocas marinas, ya que las proporciones de isótopos más pesados en las rocas indican temperaturas más frías. Al mismo tiempo es posible usar las rocas para estudiar patrones en la diversidad biológica antigua, es decir, usando el registro fósil. A partir de éste sabemos que la estrategia más común de las especies ante los cambios climáticos no es extinguirse ni adaptarse, sino moverse. Por ejemplo, el registro fósil muestra que los escarabajos se movieron mientras cambiaba el clima en el Cuaternario, mientras que no se nota tanto cambio evolutivo en la morfología ni tanta extinción de estos animales en dicho periodo. Aún más, se pueden inferir cambios en los patrones de interacción de las especies a partir de la composición de fósiles que coinciden en un lugar y un cierto periodo histórico o a partir de evidencia directa. Por ejemplo, se deduce que la herbivoría foliar causada por insectos aumenta con la temperatura porque se ve más daño debido a insectos en hojas fosilizadas en épocas más calientes.
No obstante, existen dos retos importantes en el uso del registro fósil para entender los efectos históricos de los cambios del clima en las interacciones. El primero es que el registro fósil raramente recoge una interacción en proceso, o sea, la presencia de dos organismos interactuantes en el mismo fósil; además existe el sesgo que genera el registro fósil sobre las inferencias de posibles interacciones bióticas debido a la fosilización diferencial, en la que unas especies fosilizan mejor que otras, lo cual puede generar inferencias equívocas en cuanto a la coincidencia temporal. Por ejemplo, aunque es razonable suponer que las hormigas hubieran podido ser dispersores importantes de semillas desde el periodo Terciario debido a la coincidencia temporal de ambos grupos, la evidencia de tal proceso de dispersión en el registro fósil es desproporcionadamente escasa. El segundo reto específicamente relacionado con los trópicos es el magro registro fósil de especies tropicales. Este problema se debe en parte a procesos biogeoquímicos típicos de los trópicos, incluyendo las rápidas tasas de descomposición de la materia orgánica y el mayor desgaste de las rocas. Por otra parte está el sesgo de muestreo: es más difícil de excavar y por lo tanto examinar el registro fósil tropical, lo que simplemente redunda en que es menos estudiado que el de las zonas templadas.
A pesar de las limitaciones del registro fósil, existen otras estrategias para estudiar las relaciones entre el clima y la biodiversidad del pasado. Una de ellas es el estudio de las relaciones filogenéticas entre especies o poblaciones en combinación con relojes moleculares. Este método implica investigar cambios comparativos en las secuencias genéticas entre organismos para estimar la cantidad de divergencia. El reloj molecular supone que los cambios en las secuencias de adn se acumulan a una tasa definida, lo cual permite estimar el tiempo de eventos de divergencia entre especies o poblaciones. Ya que los métodos recientes permiten calibrar la tasa de divergencia con fechas conocidas de fósiles de algún grupo particular, se pueden correlacionar los eventos de divergencia con cambios climáticos bien establecidos en el tiempo geológico. Otra estrategia es correlacionar la distribución actual de una especie con las condiciones climáticas actuales para modelar la distribución histórica o futura de la especie predicha por su nicho climático.
Una vez esbozadas las estrategias, pasemos ahora a analizar el uso de las mismas para entender los posibles efectos del cambio climático antropogénico sobre una clase de interacción de especies, la cual ha sido históricamente menos estudiada y que es muy importante para la ecología de las regiones tropicales: el mutualismo.
Mutualismo y cambio climático
El mutualismo es una interacción de dos especies o gremios de especies en donde los diferentes interactuantes se benefician de la interacción. El aprovechamiento de un mutualismo dado varía con el contexto ambiental abiótico y biótico. De hecho, cierta interacción puede ser desde muy ventajosa —en términos de adecuación para las especies involucradas— o tener consecuencias de beneficio intermedio o, incluso, los beneficios llegan a desaparecer completamente. Este gradiente de resultados puede variar geográficamente dependiendo de cuáles especies se hallan en una localidad dada en el área de distribución de los mutualistas (ya que diferentes especies ofrecen servicios mutualistas de diferentes calidades), además de cuáles rasgos morfológicos o ecológicos presentan las poblaciones locales de cada interactuante en esa ubicación particular. Dicha variación geográfica también tiene efectos importantes sobre la evolución de cada especie mutualista, un fenómeno conocido como “el mosaico geográfico de la coevolución”.
La fuerza de los efectos del cambio climático antropogénico sobre los mutualismos dependerá tanto de la facilidad y rapidez con la que las diferentes especies mutualistas se dispersan, como del grado en que una especie depende de otra u otras para su supervivencia y desempeño. Por ejemplo, algunos de los mutualismos son obligatorios, es decir, ninguna especie puede sobrevivir sin la otra. Para este tipo de mutualismo el cambio climático antropogénico puede tener efectos especialmente fuertes porque las condiciones del nicho ecológico al que se han desplazado tienen que ser apropiadas para ambos interactuantes. Cuando la manera más eficaz de reaccionar a los cambios del clima es moverse a otro lugar donde las condiciones son adecuadas, la manera en que cambiará un mutualismo obligatorio dependerá de la facilidad con la que ambas especies se dispersen a otro lugar. En este contexto es notable que una clase importante de mutualismos es la dispersión de semillas, sobre todo la dispersión de semillas por animales que comen frutos y así mueven las semillas lejos de la planta progenitora. Este es un servicio del dispersor mutualista, que disminuye el riesgo de mortalidad por enemigos naturales especializados en el consumo de las semillas que se concentran en el área ubicada bajo la copa de la planta progenitora (la cual provee frutos como recompensa al dispersor) y que también determina cuánto y dónde tales plantas se pueden mover. Así resulta que el mutualismo puede definir el potencial de que las plantas y sus dispersores respondan a los cambios climáticos.
Consideremos como ejemplo los posibles efectos del cambio climático sobre un mutualismo tropical famoso: los árboles de higo o higueras (Ficus spp., Moraceae) y sus dispersores y polinizadores. Los árboles de este género tienen una distribución pantropical y son importantes por su abundancia y su fructificación masiva, que además ocurre en varios periodos del año. Así, los árboles de higo operan como especies clave para animales frugívoros en bosques tropicales, manteniendo muchas especies de aves y monos que comen sus frutos y dispersan sus semillas. Al mismo tiempo, las flores de las higueras involucran otro mutualismo obligatorio: sus flores son polinizadas por avispas específicas (familia Agaonidae) que ponen sus huevos en los higos y transfieren el polen entre las flores. Cuando nacen las larvas se alimentan de algunas de las semillas del higo. Por medio de este mecanismo obligatorio de polinización, la respuesta de las higueras al cambio climático dependerá también de la respuesta de sus avispas polinizadoras y viceversa. Dado que las higueras en buena medida sustentan las poblaciones de una gama de frugívoros en algunos bosques tropicales, el futuro de los frugívoros a su vez dependerá de las avispas de higo (y viceversa).
Existe otro mutualismo similar al de la higuera y la avispa, pero que ocurre en zonas templadas en el sureste de los Estados Unidos: las plantas de yuca o izotes y sus polillas polinizadoras especializadas. Muy parecidas a las avispas de higo, las larvas de estas polillas también se alimentan de las semillas de las yucas. Los investigadores usaron métodos filogenéticos para investigar la historia ecológica de la interacción y cómo ésta respondió a los cambios del clima, examinando si las parejas de especies de planta y la polilla se dispersaron juntas y si tuvieron la misma historia demográfica. Los resultados mostraron que los mutualistas se expandieron juntos durante la última glaciación, hace aproximadamente doce mil años. Los autores de esta investigación proponen que el patrón congruente se debe al carácter obligatorio de la interacción. Aunque este estudio sugiere que podríamos entender la historia de muchas interacciones mediante el estudio de las filogenias, un problema es que los relojes moleculares son imprecisos, en particular en el caso de linajes de organismos que no tienen muchos fósiles para calibrar el reloj, lo cual desafortunadamente significa que son imprecisos para numerosos linajes tropicales.
Mutualismos planta-hormiga
Una clase de mutualismo que pertenece solamente a las regiones tropicales es la de mutualismo obligatorio entre plantas y hormigas, también conocido como mirmecofilia.
Es simbiótico ya que la colonia de hormigas vive dentro de los tejidos de la planta hospedera. Así, la planta y la colonia de hormigas viven en proximidad a lo largo de la vida de una o de ambas. La planta provee a las hormigas el espacio (lugar físico) para vivir y alimento, y las hormigas (en particular la casta de las obreras) defienden a la planta contra los herbívoros. De esta manera, los rasgos mutualistas de la planta son el tipo y la cantidad de espacio, y el alimento que provee; los de las hormigas son la cantidad de obreras en la colonia y su conducta defensiva. Una colonia de hormigas consiste en por lo menos una reina que produce los huevos de las hormigas obreras y las reproductivas (machos y hembras). Cuando alcanzan la madurez, las hormigas reproductivas salen de la planta hospedera para aparearse con las reproductivas de otras colonias. Los machos se mueren un poco después y las hembras buscan una nueva planta hospedera para fundar otra colonia.
Lo anterior permite ver que el cambio climático podría afectar la mirmecofilia indirectamente al cambiar la distribución del nicho fundamental de los interactuantes o directamente al cambiar los rasgos de las especies mutualistas. Es conocido que los cambios históricos en el clima han afectado la distribución de los bosques tropicales donde la mirmecofilia es prevalente. Los cambios en la distribución del hábitat afectan la biogeografía de las especies y también pueden tener efecto en los rasgos de los mutualistas y con ello en las consecuencias de la interacción. Se ha documentado un caso de esto en el mutualismo entre Leonardoxa africana y dos especies de hormigas simbióticas en África. Hacia el final del último máximo glacial, hace doce mil años, los bosques húmedos donde se despliega este mutualismo mirmecófilo se expandieron hacia el sur. Las plantas y hormigas también expandieron su distribución y esta historia es visible en la diversidad genética de la planta y de las hormigas: las especies muestran más diversidad genética en la parte norte de la distribución que en la del sur, lo cual implica que las poblaciones son más antiguas en el norte. Al mismo tiempo, las hormigas muestran un gradiente de rasgos fenotípicos: las del norte son más competitivas, pero las del sur son mejores para dispersarse y producen más hembras reproductivas que también son más grandes. Este ultimo rasgo está correlacionado con el de producir menos obreras, resultando así que las colonias del sur son peores defensoras de sus plantas mirmecófitas. Tal pérdida de beneficios en el sur podría desestabilizar el mutualismo en tiempo evolutivo, salvo que el tiempo de generación de las plantas sea mucho más largo que el de las hormigas. Además, a pesar del gradiente en los rasgos de las hormigas, las plantas mirmecófitas no muestran ningún cambio en sus rasgos hacia el sur. Con el tiempo, las hormigas del norte pueden reemplazar a las del sur por ser más competitivas, estabilizando así el mutualismo sin requerir que cambien los rasgos de las plantas.
Recientemente se ha documentado otra manera en que el clima puede afectar los rasgos de los mutualistas en mirmecofilias directamente, como lo ejemplifica un caso de este mutualismo en los bosques secos caducifolios de América Latina. El árbol Cordia alliodora (familia Boraginaceae) se distribuye desde México hasta Argentina y está asociado con hormigas simbióticas y defensoras del género Azteca a lo largo de su distribución. De manera importante, este mutualismo involucra tres interactuantes: el árbol, las hormigas y un grupo de insectos chupadores de savia tipo escama (cocsoideos, del orden Hemiptera). El árbol no provee alimento directamente las hormigas, sino indirectamente, por medio de los cocsoideos. Estos insectos chupan la savia del árbol y excretan una miel rica en azúcar, la cual es cosechada por las hormigas. Se puede modelar este mutualismo como un gran intercambio de carbono: el árbol provee carbono en forma de azúcares para las hormigas por medio de los cocsoideos y las hormigas protegen contra herbívoros las hojas de los árboles, que son las fuentes del carbono (figura 1).
A lo largo de la costa del Pacífico, desde México hasta Costa Rica, existe un gradiente latitudinal de precipitación en los bosques secos caducifolios. En Jalisco llueve anualmente casi la mitad de lo que en Guanacaste, Costa Rica (figura 1). En los sitios donde llueve menos, la época seca también es más larga, de modo que la sequía es más estresante para los árboles en México que en Costa Rica. Un punto clave es que los árboles son caducifolios, por lo que el carbono que producen y almacenan durante la época lluviosa tiene que ser suficiente para crecer, reproducirse, mantener las hormigas y sobrevivir en la época seca subsecuente. El estrés causado por las sequías más largas se refleja en la menor cantidad de carbono almacenado por los árboles a finales de la época seca en los sitios de menor precipitación, como lo es Jalisco. El costo ecológico de la herbivoría en las hojas es por tanto comparativamente más alto para los árboles de México porque tienen menos tiempo cada año para producir carbono. Si producen muy poco carbono, los árboles pueden morir de inanición. Aun así, resulta que los árboles de lugares más secos invierten más de su carbono en sus hormigas defensoras para evitar la posibilidad de daño catastrófico por la herbivoría y en consecuencia el riesgo de mortalidad por falta de carbono. Así que el patrón a lo largo de la distribución del sistema es que las colonias de hormigas cuidan un mayor número de cocsoideos y defienden mejor a los árboles en sitios con más estrés hídrico, donde llueve poco, comparado con los sitios en donde llueve más. Dado este escenario, cabe preguntarse: ¿cómo afectará el cambio climático antropogénico este mutualismo? Ya dijimos antes que es difícil saber exactamente cómo cambiará la estacionalidad y la precipitación de estos bosques, pero la evidencia indica que los eventos de precipitación del futuro, incluyendo las sequías, podrían ser más extremos. Todo esto sugiere que este mutualismo se podría fortalecer con el cambio climático antropogénico. Sin embargo, un mutualismo más intenso entre el árbol y sus hormigas podría generar consecuencias importantes, si bien difíciles de definir, para otros organismos de la comunidad ecológica (incluyendo, por ejemplo, las larvas fitófagas de alrededor de 37 especies de mariposas y polillas, las cuales como adultas son polinizadores importantes de muchas plantas, así como de escarabajos que son herbívoros del árbol). Las posibles cascadas de consecuencias de estas alteraciones ecológicas en la comunidad representan un apasionante campo de investigación que merece estudios subsecuentes.
Cambio climático y otras amenazas
El cambio climático es sólo uno de los varios cambios ambientales globales causados por la actividad humana contemporánea, y al interactuar de manera indirecta o en sinergias complejas con la deforestación, las introducciones de especies exóticas, los cambios en los nutrimentos del suelo y la defaunación de animales vertebrados e invertebrados, generará efectos muy poco predecibles en la biodiversidad global. Por ejemplo, la red actual de áreas protegidas en Madagascar no permitirá a los carismáticos árboles baobab moverse en concierto con los cambios del clima, como hubiera podido ocurrir sin los niveles actuales de deforestación. Es indudable que esto tendrá consecuencias complejas sobre la red de especies mutualistas y antagonistas de estos árboles pero, nuevamente, nuestra capacidad de predecir los detalles relevantes es aún muy limitada.
Por otra parte, todavía carecemos de la investigación necesaria que conecte los múltiples servicios derivados del ecosistema que los humanos necesitamos para sobrevivir (agua, alimento, madera, regulación del clima, etcétera) con la biodiversidad en general y las interacciones de especies en particular. Enfatizamos que esta investigación, si bien importante en todos los biomas, será particularmente esencial en los trópicos, donde existe la mayoría de la biodiversidad planetaria. Valorar la importancia de tales estudios y la difusión de los resultados de los mismos serán aspectos adyuvantes de cara a los desafíos que nos presenta el antropoceno.
|
||||||||||||
|
Referencias Bibliográficas
Blatrix, Rumsaïs, Doyle McKey y Céline Born. 2013. “Consequences of past climate change for species engaged in obligatory interactions”, en Comptes Rendus Geoscience, vol. 345, núm. 78, pp. 306-315.
Dirzo, Rodolfo, et al. 2014. “Defaunation in the Anthropocene”, en Science, vol. 345, núm. 6195, pp. 401-406. Kiers, E. Toby, et al. 2010. “Mutualisms in a changing world: an evolutionary perspective”, en Ecology Letters, vol. 13, núm. 12, pp. 1459-1474. Léotard, Guillaume, et al. 2009. “Range expansion drives dispersal evolution in an equatorial threespecies symbiosis”, en plos one, núm. 4, pp. 1-11. Pounds, J. Alan, et al. 2006. “Widespread amphibian extinctions from epidemic disease driven by global warming”, en Nature, núm. 439, pp. 161-167. Pringle, Elizabeth G., et al. 2013. “Water stress strengthens mutualism among ants, trees and scale insects”, en plos Biology, núm. 11, pp. e1001705. Renton, Katherine y Alejandro SalinasMelgoza. 2004. “Climatic variability, nest predation, and reproductive output of lilaccrowned parrots (Amazona finschi) in tropical dry forest of western Mexico”, en The Auk, vol. 121, núm. 4, pp. 1214-1225. Sinervo, Barry, et al. 2010. “Erosion of lizard diversity by climate change and altered thermal niches”, en Science, vol. 328, núm. 5980, pp. 894-899. Smith, Christopher I., et al. 2011. “Comparative phylogeography of a coevolved community: concerted population expansions in Joshua trees and four yucca moths”, en plos one, vol. 6, núm. 10, pp. e25628. Tylianakis, Jason M., et al. 2008. “Global change and species interactions in terrestrial ecosystems”, en Ecology Letters, vol. 11, núm. 12, pp. 1351-1363. |
||||||||||||
| _____________________________ |
||||||||||||
| Elizabeth Pringle University of Michigan. Estados Unidos. Estudió ciencias ambientales y políticas públicas en la Universidad de Harvard y su doctorado en biología en la Universidad de Stanford. Se interesa en la ecología evolutiva de las interacciones de las especies, incluyendo plantas, animales y microbios. Actualmente es investigadora en la Universidad de Michigan. Rodolfo Dirzo Stanford University, Estados Unidos. Estudió biología en la Universidad Autónoma de Morelos; la maestría y el doctorado en la Universidad de Gales, estudió la ecología evolutiva de la relación entre plantas y animales. Ha sido investigador en la Universidad Nacional Autónoma de México en los institutos de Biología y Ecología y fue director de la Estación de Biología Tropical “Los Tuxtlas”. Actualmente es profesor en el Departamento de Biología de la Universidad de Stanford. |
||||||||||||
| _____________________________ | ||||||||||||
|
cómo citar este artículo →
Pringle, Elizabeth G. y Rodolfo Dirzo. 2016. Efectos del cambio climático antropogénico en las interacciones mutualistas de especies tropicales. Ciencias, núm. 120-121, abril-septiembre, pp. 4-16. [En línea].
|
||||||||||||
| del herbario |
|
|||||||||||||
|
El hallazgo de Isoetes
en Guerrero: plantas chapadas a la antigua |
 |
|||||||||||||
|
Ernesto Velázquez Montes
|
||||||||||||||
|
Corría el año 1998, el 15 de diciembre para ser exacto,
cuando con mi amigo Eduardo llegué por primera vez a un lugar muy cerca del pueblo Monte Alto, Municipio de San Marcos, en la Costa Chica del estado de Guerrero. Andábamos en plan de trabajo como biólogos, buscando plantas, recolectándolas para estudiarlas, conocer su nombre científico, entre otras cosas, pues el objetivo era determinar toda la flora del estado de Guerrero. En particular buscábamos plantas que viven en charcos, de las llamadas acuáticas, pues a él le interesaban ya que estaba haciendo su tesis de maestría. Era el penúltimo día de trabajo y nuestro trayecto había sido largo; salimos de la ciudad de México el 8 de diciembre, atravesamos toda la Sierra Madre del Sur, subimos por el pueblo de Mezcala, ubicado en la cuenca del río Zopilote, pasamos por Filo de Caballos hasta llegar a Atoyac, ubicado en la Costa Grande, para dirigirnos hacia Acapulco y llegar cerca de San Marcos, ya en la Costa Chica.
Aún recuerdo muy bien ese día. Cuando tomamos la desviación de terracería a Monte Alto eran alrededor de las cinco de la tarde y, aunque sabíamos que teníamos ya poco tiempo con luz (porque los días en esas fechas son cortos) y además no conocíamos el lugar, nos animamos a explorarlo y ver si se encontraban las plantas que buscábamos. Recorrimos en la camioneta alrededor de siete kilómetros cuando vimos un gran charco a la izquierda del camino, así que nos paramos y empezamos a buscar. Fue grande nuestra alegría al comprobar que sí se encontraban las plantas que buscábamos, conocidas como alismatáceas. Mientras él las recolectaba y preparaba para llevárnoslas, me aparté para ver si encontraba otras diferentes, pues estaba en mi mente la posibilidad de encontrar particularmente el género Marsilea, que son helechos acuáticos parecidos a un trébol de cuatro hojas, pues las condiciones ecológicas del lugar eran las idóneas para que creciera ahí.
Conforme pasó el tiempo fui perdiendo la ilusión de encontrar los helechos; estaba a punto de oscurecer y casi no se distinguían las plantas. Decidí no buscar más y me detuve en la orilla del charco porque tuve la necesidad de orinar. Estaba yo concentrado en dicho asunto, cuando llamaron mi atención unas plantitas de unos cuantos centímetros de altura y que estaban justo allí, medio sumergidas en el agua; tenían mal aspecto, parecía que las pisaron los animales, y sí, había muchas huellas cerca de ellas. A primera vista me pareció que eran pastos; sin embargo, algo tenían que llamaron mi atención. Cuando terminé con lo que me ocupaba, me puse de rodillas para verlas de cerca y tuve que meter mis manos al agua para sacar una con la raíz y examinarla de cerca. No había duda, se trataba de plantas del género Isoetes, las cuales son muy escasas y raras, no sólo en México, sino en todo el mundo. Dicho hallazgo me provocó una extraña mezcla de sentimientos: por un lado alegría pero también incredulidad, después de más de veinte años de andar recolectando plantas en todo el estado ¡no lo podía creer, había encontrado Isoetes en Guerrero! Era un hallazgo importante pues, como mencioné, son muy escasas. Nos cayó la noche dando brincos de alegría y emoción, fuimos a hospedarnos a San Marcos y al otro día partimos de regreso a la ciudad de México, finalizando así nuestro trabajo en Guerrero.
El género Isoetes
Son hierbas pequeñas que, dependiendo de la especie, miden entre 10 y 50 cm de largo, y algunas excepcionales pueden llegar a medir un poco más. En su morfología general son parecidas a las cebollitas cambray o a un maguey pequeño, aunque sus hojas son más delgadas y se parecen mucho a las de algunos pastos; también suelen confundirse con otras plantas dulceacuícolas conocidas como ciperáceas y juncáceas. Así, las plantas de Isoetes viven en charcos, ya sea sumergidas completamente en el agua en la época de lluvias o conforme se acerca la época seca la parte superior de sus hojas sale del suelo, lo demás, es decir, sus raíces, su reducido tallo y la parte inferior de sus hojas quedan enterrados en el lodo; ya en plena época de secas, al menos en la población de Guerrero, las plantas desaparecen completamente, permaneciendo en el suelo sólo sus esporas, las cuales germinan en la siguiente época de lluvias, restableciéndose así su ciclo de vida. Las plantas de Isoetes de Monte Alto no miden más de 35 cm de largo, sus hojas son como listones, largas y delgadas con una sola vena central, en su interior tienen cuatro cavidades llenas de aire y septadas transversalmente, las cuales recorren a todo lo largo la vena central; no tienen semillas, pero sí esporas que son de dos tipos: microsporas y megasporas, las cuales nacen por separado en los esporangios que se encuentran en las bases internas de las hojas. Sus tallos son tan pequeños que casi del mismo sitio donde nacen las hojas salen las raíces, de tal manera que se puede decir que estas plantas prácticamente no tienen tallo, como ocurre con las cebollas y los magueyes, pero a una escala más reducida.
La historia de Isoetes
El género Isoetes pertenece a la división Lycophyta, que se conocen como licopodios de los cuales muy pocos viven en la actualidad, pues muchos son fósiles; son plantas muy antiguas, que tuvieron su origen hace aproximadamente 400 millones de años, en el Devónico inferior (cuadro 1).
Las especies de Isoetes son parientes lejanos de los fósiles del género Lepidodendron, los cuales fueron árboles con alturas hasta de 40 metros y formaron bosques muy extensos durante el Carbonífero, hace alrededor de 300 millones de años. Los especialistas en estudiar las plantas fósiles, los paleobotánicos, han estimado que dichos bosques llegaron a cubrir superficies de varios cientos de hectáreas, por lo que eran parte importante de la vegetación. Esos bosques y especies fueron desapareciendo, pero algunos de sus descendientes sobrevivieron, cambiando, de tal manera que se fueron reduciendo de tamaño. De aquellos enormes árboles hoy en día sólo quedan las pequeñas y delicadas hierbas conocidas como Isoetes; son sus últimos representantes.
Chapadas a la antigua
Todas las especies de Isoetes conservan hasta la actualidad algunas características anatómicas, fisiológicas y morfológicas de sus ancestros. Dichas características las hacen ser un poco diferentes a todas las plantas que hay en la actualidad; por ejemplo, a pesar de ser hierbas de tallas pequeñas, aún conservan en su reducido tallo vestigios de la anatomía leñosa de sus ancestros arbóreos Lepidodendron (un conjunto de células que tienen crecimiento secundario anómalo, por lo que Yudzuru Ogura, un anatomista de pteridofitas, lo ha denominado como “tejido prismático”).
Otra característica particular de Isoetes es su mecanismo para realizar fotosíntesis, el cual se conoce como cam por sus siglas en inglés y traducido al español significa Metabolismo Ácido Crasuláceo, y que lo presentan muy pocas plantas en el mundo, como las suculentas, pero también epífitas como orquídeas y bromelias, y permite que las plantas capturen el dióxido de carbono (CO2) por la noche, a diferencia de la mayoría de las plantas, que lo hacen durante el día. Isoetes hace la captura de CO2 de dos maneras: una es a través de sus raíces huecas, de donde se difunde hacia las cuatro cavidades que corren a todo lo largo de la hoja; la otra es por sus estomas, que son pequeñas estructuras en la epidermis de las hojas que tienen la capacidad de abrir o cerrar dependiendo del estado fisiológico de la planta. Cabe mencionar que no todas las especies de Isoetes tienen estomas; la especie de Guerrero sí los presenta. De manera general se considera que el metabolismo cam es una adaptación de las plantas para vivir en ambientes secos, ya que les permite almacenar agua en sus tejidos; sin embargo, las plantas del género Isoetes son una excepción a esta regla, ya que no viven en sitios secos ni almacenan agua, pero lo presentan porque al capturar el CO2 durante la noche evitan la competencia con las otras plantas acuáticas que tienen el metabolismo CO3 y lo capturan durante el día.
Otra característica de Isoetes que llama la atención es que siendo plantas con dos tipos de esporas (microsporas y megasporas) en lugar de producir cuatro megasporas en cada megasporangio como lo hacen todas las plantas de este tipo, produce varias decenas o cientos de megasporas en cada megasporangio, lo cual es considerado como primitivo. Además, las megasporas de Isoetes son triletes, es decir, tienen tres cicatrices que forman una “Y”, correspondientes a las líneas en donde abre la espora cuando germina, mientras que sus microsporas son monoletes, es decir, tienen sólo una cicatriz, una combinación presente únicamente en este grupo de plantas.
Importancia del hallazgo
La especie que se encontró en Monte Alto, Guerrero, recibe el nombre científico de Isoetes pallida Hickey y su hallazgo es importante porque es endémica de México. Hasta hoy, solamente se ha encontrado en los estados de Campeche, Guerrero y Oaxaca, lo que indica que tiene una distribución muy restringida y, por lo tanto, es necesario implementar estrategias para su conservación.
A estas plantas todavía no se les ha encontrado un uso que beneficie directamente a las personas, es decir, no se comen, no son medicinales, no se usan para ningún ritual ni sirven como alimento para el ganado porque son muy pequeñas, etcétera; sin embargo, desde el punto de vista biológico son muy importantes. Primero, porque representan los últimos restos de un grupo de plantas muy antiguo; y segundo, porque como todo ser vivo, tienen un papel ecológico importante, ya que están relacionadas con otras plantas y animales (muy probablemente animales pequeños que se alimentan o interaccionan con ellas), de tal manera que forman parte de una cadena ecológica importante para la conservación de la riqueza biológica de la región.
En el caso particular de las plantas de Guerrero, aunque no se han realizado estudios ecológicos que permitan saber más de su biología, se ha estimado a priori como una población vulnerable, pero después de hacer otros estudios, dadas las condiciones en las que se encuentran, pudiera estar en la categoría “en peligro de extinción” de acuerdo con los criterios de la Unión Internacional para la Conservación de la Naturaleza o la Secretaría del Medio Ambiente y Recursos Naturales.
El problema es que en cada época de lluvias no hay más de cincuenta individuos por hectárea y una parte de éstos es pisoteada por el ganado, lo que podría significar que no lleguen a madurar sus esporas; asimismo, es muy probable que también les afecte el uso de herbicidas que se utilizan para desyerbar los terrenos.
Proteger la población
Es necesario informar a los pobladores y a las autoridades de Monte Alto y San Marcos, que son los pueblos más cercanos donde vive Isoetes pallida, para que conozcan la situación e implementen medidas de protección, como cercar el lugar y vigilarlo, para impedir que el ganado u otro tipo de animales las dañen. Otra acción sería evitar el uso de herbicidas, pues el daño que causan a las plantas los compuestos químicos es irreversible y ponen en peligro su existencia.
También es importante informar a la comunidad científica para que realicen otro tipo de estudios, comenzando por los ecológicos, lo que permitirá determinar con más certeza su estado de conservación, pero también los fisiológicos, genéticos y moleculares. Urge evitar que desaparezcan.
|
||||||||||||||
|
Referencias bibliográficas
Mehltreter, K., L. R. Walker y J. M. Sharpe (eds.). 2010. Fern ecology. Cambridge University Press, Cambridge. Mendoza Ruiz, A. y B. Pérez García. 2009. Helechos y Licopodios de México. conabio-uamiz, México. Mickel, John T. y Alan Reid Smith. 2004. The pteridophytes of Mexico. Memoirs of the New York Botanical Garden. New York Botanical Garden, Nueva York. Pigg, K. B. 2001. “Isoetalean lycopsid evolution: from the Devonian to the present”, en American Fern Journal, vol. 91, núm. 3, pp. 99-114. Ranker, Tom A. y Christopher H. Haufler (eds.). 2008. Biology and evolution of fern and lycophytes. Cambridge University Press, Cambridge. Riba, R. y B. Pérez García. 1997. “¿Pueden las pteridofitas ser árboles?”, en Revista Contactos, núm. 24, pp. 5-9. Taylor, Thomas N., Edith L. Taylor y Michael Krings. 2009. Paleobotany. The Biology and evolution of fossil plants. Elsevier, Nueva York. |
||||||||||||||
| _______________________________________________ | ||||||||||||||
| Ernesto Velázquez Montes Facultad de Ciencias, Universidad Nacional Autónoma de México. |
||||||||||||||
| _________________________________________________ | ||||||||||||||
|
cómo citar este artículo →
Velázquez Montes, Ernesto. 2016. El hallazgo de Isoetes en Guerrero: plantas chapadas a la antigua. Ciencias, núm. 120-121, abril-septiembre, pp. 98-101. [En línea].
|
||||||||||||||
| del clima |
|
|||||||||||||
|
El Niño,
el Usumacinta y el Grijalva |
 |
|||||||||||||
|
Esperanza Muñoz Salinas
|
||||||||||||||
|
Los ríos Usumacinta y Grijalva son los más caudalosos
de México; ambos nacen en la Sierra de los Cuchumatanes en Guatemala y en los primeros kilómetros de su recorrido transitan por su país natal para luego introducirse en México, discurriendo por el estado de Chiapas. Muy pronto el río Grijalva penetra en la zona montañosa, mientras que el Usumacinta la rodea. Los dos afluentes desembocan juntos en Tabasco pues, unos kilómetros antes de alcanzar el Golfo de México, se reúnen. Estos ríos constituyen un sistema fluvial que drena una superficie de más de cien mil km2, lo que equivale a 5% de la extensión de la República Mexicana; debido a las altas precipitaciones que reciben las zonas por las que discurren, su capacidad de transporte de agua y sedimentos es muy alta, lo cual se traduce en una fuerte modificación del relieve del territorio por el que se mueven y ésta se incrementa o disminuye a capricho de El Niño.
Cuando se menciona el fenómeno de El Niño, casi de manera instantánea se nos viene a la mente la imagen de un pequeño de pocos años; de hecho, si atribuimos características humanas a este fenómeno podríamos considerar que a veces hasta hace travesuras. El nombre de esta anormalidad climática hace alusión al Niño Dios debido a que la primera vez que se identificó se relacionó con un reverdecimiento de la flora en la costa árida de Perú, un hecho más o menos coincidente con las fechas en las que se celebra el nacimiento de Jesucristo en el cristianismo. Aunque se sabe que El Niño es un fenómeno físico que afecta al medio natural a escala global, todavía no se conocen exactamente los mecanismos que lo generan.
Efectos en el mar
Las peculiaridades que caracterizan a El Niño se manifiestan en el clima. Los periodos que tiene este fenómeno se determinan por la temperatura que se registra en la superficie de los océanos. ¿Cómo se mide la temperatura superficial de los océanos? Consideremos una columna vertical en la masa de agua localizada en el interior
de cualquier océano; la parte más superficial estará en contacto con el aire atmosférico y la parte más profunda tocará el fondo del océano. La longitud de esta columna vertical de agua puede fluctuar desde decenas de metros a más de una decena de kilómetros, según en qué punto del océano nos encontremos, pues existen irregularidades en el relieve de la cuenca oceánica. Sin embargo, a pesar de los cambios en la profundidad de la columna vertical, siempre encontraremos un patrón similar respecto de la temperatura oceánica: los primeros metros de la columna o superficie oceánica se encuentran en contacto con el aire atmosférico y el agua recibe la radiación solar, la temperatura (de aproximadamente 17 °C) es considerablemente más alta que en el resto y, a mayores profundidades, se registran temperaturas por debajo de 0 °C.
Debido a que la medición de la temperatura en la superficie oceánica depende de los distintos procedimientos empleados por la institución que realiza dichas medidas, ha sido difícil homogeneizar a nivel mundial los umbrales a los cuales se presenta una anomalía en la temperatura por debajo de tal superficie oceánica. Actualmente, y de manera más extendida, se considera que el fenómeno de El Niño se puede detectar cuando existe un incremento en la temperatura media de la superficie oceánica por encima de 0.5 °C durante al menos cinco meses consecutivos, esto en el océano Pacífico y entre los paralelos 5° norte y 5° sur. Existen dos puntos dentro de esta franja del océano que se encuentran en Darwin, Australia y en Tahití, Polinesia Francesa, los cuales son especialmente sensibles a los cambios de temperatura y es por ello que se les toma como medidas de referencia.
También se sabe que este calentamiento en la superficie del agua guarda relación con una serie de corrientes marinas que permiten la mezcla del agua de todos los océanos, por estar interconectados. La circulación global oceánica homogeneiza la temperatura de todas las masas de agua y su salinidad. Aunque la temperatura varía en la superficie oceánica de manera estacional y diaria, lo que condiciona las corrientes marinas es el cambio de temperatura debido a la posición latitudinal del océano, ya que la radiación solar se reduce desde el ecuador hacia los polos y la temperatura es proporcional a la radiación absorbida en la superficie oceánica. De esta manera, el agua en los polos está más fría que en el ecuador y por ello existen corrientes entre estos puntos. Como el agua fría es más densa que la caliente, la primera desciende por debajo de la segunda. Así, las corrientes frías se distribuyen bajo la superficie del océano y no se mezclan ni con el agua que se encuentra en superficie ni con el resto del agua que existe a mayor profundidad en la columna de agua oceánica. Por ello en las profundidades del océano se pueden registrar distintas temperaturas del agua según las corrientes que tengan lugar.
Respecto de la salinidad, ésta depende principalmente de la evaporación que existe en la superficie del océano, la cual está determinada nuevamente por la radiación solar. De esta manera, en el ecuador el agua tiene mayor concentración de sales que en los polos, sin embargo, se considera que la circulación global oceánica está principalmente definida por los cambios de temperatura entre los polos y el ecuador, aunque un cambio de salinidad podría generar una modificación del régimen de la circulación global oceánica.
Ya que la circulación global oceánica guarda una estrecha relación con la radiación solar, entonces podemos deducir que ésta presenta un paralelismo con el modelo de circulación atmosférica que controla el clima terrestre. Así, al igual que los océanos exhiben corrientes marinas para homogeneizar la temperatura oceánica, la atmósfera manifiesta corrientes de aire para mezclar los vientos calientes con los fríos. Ambas corrientes circulan desde los polos al ecuador y viceversa, y además están subordinados al movimiento de rotación de la Tierra.
De lo dicho anteriormente se deduce que en la zona oceánica ubicada entre los paralelos 5° norte y 5° sur del océano Pacífico (donde se miden los cambios de temperatura sobre la superficie del océano para identificar el fenómeno de El Niño) las corrientes se dirigen desde el oeste, en las costas de Indonesia y Australia, hacia el oeste, en las costas situadas al sur del continente americano a la altura de Perú. Un incremento en la temperatura de dicha corriente a tal latitud repercute en un cambio no sólo en la vegetación y la fauna acuática de las costas a las que afecta, sino que también guarda una estrecha relación con la temperatura del aire. De esta manera el clima también se modifica. Mientras que en las costas americanas durante El Niño generalmente se incrementan las precipitaciones, en las costas de Asia y Australia se presentan periodos de sequía.
Cabe mencionar que existe un fenómeno antagónico a El Niño conocido como La Niña, el cual se detecta por un descenso en la temperatura media de la superficie del océano Pacífico (0.5 °C), provocando que la costa americana sea más fría y la asiática más cálida de lo normal.
El efecto en los ríos
Como la circulación global oceánica y la atmosférica tienen un efecto a escala terrestre, los cambios que ocurren en la zona del Pacífico entre los paralelos 5° norte y 5° sur también producen modificaciones en el régimen climático y oceánico en otras partes del planeta; los ríos Usumacinta y Grijalva, que se encuentran a una latitud por encima del paralelo 5° norte, también sufren durante El Niño y La Niña una alteración en su régimen de descarga de agua y sedimentos, ya que están controlados por el clima.
Debido a que tales ríos son los más caudalosos de México y que una parte importante de población mexicana vive cerca de sus cauces es importante determinar la influencia que tiene El Niño sobre ellos, pues un cambio en su régimen hidrológico puede alterar la vida de la gente de estas comunidades.
Existe en México una red de estaciones de aforo (útiles para medir el caudal y el nivel de los ríos) localizados en los cauces de los principales torrentes de México cuya gestión la realiza la Comisión Nacional del Agua.
Dichas estaciones de aforo consisten generalmente en unas secciones de corte en los cauces del río que constan de dimensiones conocidas para medir la altura de la columna de agua diariamente y calcular la descarga del río. En esa misma sección se recolecta parte del sedimento que transporta el flujo de agua, el cual se seca y pesa para calcular la descarga de sedimento del río.
A lo largo del tramo final de los ríos Usumacinta y Grijalva, antes de su confluencia, se localizan cuatro estaciones de aforo que recopilan series temporales. Estos registros comienzan alrededor de 1950 y están disponibles los datos de descarga de agua y sedimento de manera casi continua hasta el momento actual. Las mediciones de temperatura sobre la superficie del océano Pacífico en Darwin y Tahití comenzaron también a documentarse en el año 1950 y los registros se mantienen sin interrupción hasta ahora; están disponibles en la red y los publica la Administración Nacional Oceánica y Atmosférica de los Estados Unidos.
Del estudio estadístico de estos datos recopilados por más de sesenta años se deriva que durante los meses de El Niño y de La Niña la descarga en los ríos Usumacinta y Grijalva se eleva sustancialmente respecto del resto del año. Algunas de estas descargas han sido tan considerables que se han registrado inundaciones importantes en algunas poblaciones localizadas en las proximidades de los ríos Usumacinta y Grijalva, como es el caso de Villahermosa, Tabasco.
Aunque no es posible determinar con exactitud cuándo puede tener lugar una inundación que afecte catastróficamente a una determinada población, el estudio de la relación entre los cambios de temperatura en la superficie del océano Pacífico y las descargas de agua y sedimento en los ríos Usumacinta y Grijalva pone de manifiesto que las relaciones entre fenómenos físicos de distinta índole guardan una estrecha relación a nivel global.
Todavía no se conocen los mecanismos que rigen muchos de los fenómenos físicos que operan sobre la superficie terrestre, como el caso de El Niño y su influencia en los dos ríos más caudalosos de México, pero se siguen haciendo observaciones y experimentos para poder conocer un poco mejor la naturaleza de los fenómenos que se presentan en el planeta que habitamos.
|
||||||||||||||
| _______________________________________________ | ||||||||||||||
| Esperanza Muñoz Salinas Instituto de Geología, Universidad Nacional Autónoma de México. |
||||||||||||||
| _________________________________________________ | ||||||||||||||
|
cómo citar este artículo →
Muñoz Salinas, Esperanza. 2016. El niño, el Usumacinta y el Grijalva. Ciencias, núm. 120-121, abril-septiembre, pp. 18-21. [En línea].
|
||||||||||||||
| del bestiario |
|
|||||||||||||
|
Epidemia
en las cuevas de hibernación de los murciélagos |
 |
|||||||||||||
|
Diego Montañez de Azcué y Lorena A. Tzab Hernández
|
||||||||||||||
|
A finales del invierno de 2006 casi toda una colonia
de murciélagos fue encontrada muerta en Howe Caverns, una cueva turística al este de Nueva York. Dicho fenómeno se estuvo repitiendo y expandiendo año con año, siempre al final del invierno, en la región noreste de Estados Unidos, hasta septiembre de 2014, cuando fue reportada la muerte masiva de murciélagos en cuevas y minas abandonadas de veinticinco estados de Estados Unidos y cinco provincias de Canadá. Se calcula que en total han muerto 5.7 millones de murciélagos, provocando la desaparición de hasta 100% de sus poblaciones en algunos sitios. Al estudiar los afectados se pudo observar que todos pertenecen a especies que recurren a la hibernación y sus cuerpos presentan crecimientos blancos algodonosos alrededor de sus orejas, alas y hocicos, por lo que el fenómeno fue bautizado como Síndrome de la nariz blanca. Durmiendo con el enemigo
En un inicio, se pensó en alguna sustancia tóxica en el ambiente que pudiera estar enfermando y matando a los murciélagos; pero desde 2009 se reconoció el hongo Pseudogymnoascus destructans (anteriormente Geomyces destructans) como el agente causante de las muertes. Se trata de un hongo psicrófilo, esto es, que habita en lugares fríos, parásito exclusivo de la piel de murciélagos, que produce esporas muy curvadas, las cuales germinan mientras los murciélagos hibernan, ya que es durante el periodo invernal cuando el hongo encuentra las condiciones ambientales ideales para desarrollarse.
La hibernación es la facultad que poseen muchos animales para adaptarse a las duras condiciones climáticas del invierno, como el frío y la escasez de alimento, y se caracteriza por largos periodos de sueño profundo, despertares escasos e intermitentes y un aumento de hasta 27% de la masa corporal. Esta estrategia es muy importante para la supervivencia de los murciélagos, pero desafortunadamente también proporciona un escenario óptimo para el desarrollo del parásito, debido a que tales condiciones implican una reducción en las funciones inmunológicas de los animales, una disminución en la temperatura corporal, la selección de áreas húmedas para dormir y la formación de agrupaciones grandes y densas que facilitan el contagio. El hongo únicamente se contagia por contacto, ya sea entre un individuo sano y uno enfermo o entre un individuo sano y una superficie con las esporas del hongo. Cuando un murciélago se contagia, las esporas germinan y las hifas crecen, invaden y destruyen sus folículos capilares y las glándulas de su piel.
A pesar del nombre de la enfermedad, el mayor daño provocado por el hongo ocurre en las alas. Además de permitirles volar, las alas de los murciélagos juegan un papel muy importante en el mantenimiento de su metabolismo. A través de ellas ocurre el intercambio gaseoso que complementa la respiración pulmonar, el equilibrio de la temperatura y de la cantidad de agua en el cuerpo. Por consiguiente, al sufrir un daño extremo, dichas funciones se ven alteradas o interrumpidas; el murciélago se deshidrata y presenta variaciones anormales en su temperatura corporal.
La deshidratación es uno de los principales síntomas; en consecuencia, el murciélago se ve forzado a despertar muy frecuentemente de su hibernación para satisfacer sus necesidades de beber. En ocasiones se ve obligado a salir de su refugio en busca de agua, incluso durante el día, y llega a comer nieve o lamer hielo para saciar su sed. Entre 80 y 90% de sus reservas nutricionales, originalmente acumuladas para sobrevivir sin alimento durante la hibernación, es consumida por esos despertares y búsquedas de agua. Las condiciones invernales hacen que los murciélagos no cuenten con los recursos alimenticios suficientes para compensar el gasto prematuro de energía y, finalmente, mueren por inanición.
Al término de cada temporada invernal, muy pocos son los individuos que logran sobrevivir a las condiciones deplorables en las cuales el parásito los obligó a vivir. No obstante, el daño en las alas y el estado físico llega a ser tan grande que difícilmente pueden salir en busca de alimento.
De Europa a Norteamérica
En Estados Unidos existen cuarenta y siete especies de murciélagos, de las cuales más de la mitad recurren a la hibernación, lo que las pone en peligro de ser víctimas del síndrome de la nariz blanca. Al día de hoy, once especies han sido perjudicadas; entre ellas Eptesicus fuscus, Myotis grisescens, M. leibii, M. septentrionalis, M. sodalis, M. velifer y Perimyotis subflavus. Myotis lucifugus es de las más afectadas, su población total se ha reducido en casi 80% y se estima su extinción regional en diecisiete años.
Un hecho en apariencia alarmante fue la presencia de murciélagos con los mismos síntomas en Europa reportada en 2010, y el hongo responsable fue identificado como la misma especie que está devastando a los murciélagos norteamericanos. Pseudogymnoascus destructans se reportó en varias ocasiones en por lo menos quince países europeos, destacando su abundancia en Alemania, Francia y República Checa. Si bien estos datos demuestran la presencia y amplia distribución del hongo en Europa, en ese continente no existen muertes masivas, los murciélagos infectados sobreviven al invierno y las poblaciones permanecen sanas y en números constantes; ¿por qué la enfermedad es mortal en Estados Unidos y Canadá y no en Europa?
Existen diversas respuestas para explicar este contraste, pero la más probable y aceptada es la siguiente: el hongo es originario de Europa, lo cual implica que los murciélagos europeos han estado en constante convivencia con él, logrando adaptarse al fortalecer sus defensas, lo cual evita que los perjudique al grado de matarlos. Por otro lado, se sugiere que el hongo fue introducido recientemente a Estados Unidos y Canadá; los murciélagos americanos nunca, en toda su historia evolutiva, se han enfrentado a él y por consiguiente no cuentan con las defensas necesarias para combatirlo.
El turismo y la investigación en cuevas son actividades practicadas por muchas personas alrededor del mundo, por lo tanto, se sugiere que el hongo fue introducido por algún visitante, quien accidentalmente portó y trasladó las esporas del hongo desde Europa hasta la primera cueva afectada en Nueva York (probablemente en la ropa o el calzado que acostumbra usar en sus expediciones).
Acciones ante la emergencia
Las consecuencias que la desaparición de grandes cantidades de murciélagos podría traer al ecosistema son devastadoras, empezando con la disminución del control de poblaciones de los insectos que se alimentan. Muchos de esos insectos son plaga para cultivos, por lo que existen estimaciones que indican pérdidas para la agricultura de hasta 3.7 mil millones de dólares anuales.
En vista de ello, la Comisión de Pesca y Vida Silvestre de Estados Unidos implementa protocolos de descontaminación para visitantes de cuevas: clausuró ya por completo algunas cuevas turísticas en donde la plaga está presente y ha invertido 1.3 millones de dólares en el desarrollo de proyectos que buscan investigar y controlar la mortandad de los murciélagos.
La organización Bat Conservation International creó el Fondo para responder a la emergencia del síndrome de la nariz blanca. Por medio de diferentes instituciones y del público en general ha recaudado más de 65 mil dólares para financiar investigaciones al respecto, entre las cuales se incluyen pruebas con compuestos antifúngicos y el desarrollo de vacunas. Otra medida fomentada por la organización es el cuidado en cautiverio de los sobrevivientes; con las atenciones adecuadas, un murciélago sumamente dañado es capaz de regenerar sus alas y librarse por completo del hongo, pero no está del todo exento de recaer durante la siguiente temporada invernal.
Algunas propuestas, un poco más drásticas, consisten en la construcción de cuevas artificiales para que las colonias hibernen o en desinfectar las cuevas naturales antes de cada invierno, lo que podría traer graves consecuencias para el equilibrio de otros organismos que habitan en las cuevas, desencadenando más problemas que soluciones.
Una página en la red (whitenosesyndrome.org) fue creada con la finalidad de brindar a la sociedad información actualizada sobre investigaciones, nuevos descubrimientos, casos reportados y los diversos esfuerzos llevados a cabo por diferentes organismos e instituciones para controlar la enfermedad.
Aunque no se sabe cuándo el hongo podría llegar hasta México, es prudente aplicar, desde ahora, medidas de desinfección adecuadas en equipos y ropa de expedición e investigación en cuevas para reducir la probabilidad de su expansión.
Los límites ecológicos y geográficos del síndrome de la nariz blanca aún no están establecidos, por lo que se considera que todo murciélago que hiberna en el continente americano está en constante peligro, año con año, conforme se acerca el invierno.
|
||||||||||||||
| Referencias bibliográficas Blehert, David S. et al. 2011. “Bat white-nose syndrome in North America”, en Microbe, vol. 6, núm. 6, pp. 267–273. Gargas, A. et al. 2009. “Geomyces destructans sp. nov. associated with bat white-nose syndrome”, en Mycotaxon, núm. 108, pp. 147-154. Meteyer, Carol U. et al. 2009. “Histopathologic criteria to confirm white-nose syndrome in bats”, en J. Vet. Diagn. Invest., núm. 21, pp. 411–414. Minnis, Andrew M. y Daniel L. Lindner. 2013. “Phylogenetic evaluation of Geomyces and allies reveals no close relatives of Pseudogymnoascus destructans, comb. nov., in bat hibernacula of eastern North America”, en Fungal Biology, vol. 117, núm. 9, pp. 638–649. Puechmaille, Sébastien J. et al. 2011. “White-nose syndrome: is this emerging disease a threat to European bats?”, en Trends in Ecology and Evolution, vol. 26, núm. 11, pp. 570–576. Reeder, DeeAnn et al. 2012. “Frequent arousal from hibernation linked to severity of infection and mortality in bats with white-nose syndrome”, en plos one, vol. 7, núm. 6. Warnecke, Lisa et al. 2012. “Inoculation of bats with European Geomyces destructans supports the novel pathogen hypothesis for the origin of white-nose syndrome”, en pnas, vol. 109, núm. 18, pp. 6999–7003. En la red goo.gl/AlQhge |
||||||||||||||
| _______________________________________________ | ||||||||||||||
| Diego Montañez de Azcué Lorena A. Tzab Hernández Proyectos de innovación, Grupo Clustar, Mérida, Yucatán. |
||||||||||||||
| _________________________________________________ | ||||||||||||||
|
cómo citar este artículo →
Montañez de Azcué, Diego y Tzab Hernández Lorena A. 2016. Epidemia en las cuevas de hibernación de murciélagos. Ciencias, núm. 120-121, abril-septiembre, pp. 42-45. [En línea].
|
||||||||||||||